
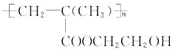 ,它是制作软质隐形眼镜的材料.请写出下列有关反应的化学方程式:
,它是制作软质隐形眼镜的材料.请写出下列有关反应的化学方程式: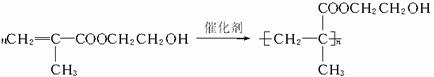 .
.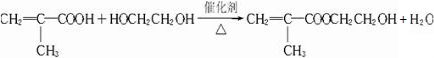 .
. .
. 分析 (1)甲基丙烯酸羟乙酯含碳碳双键,发生加聚反应生成聚甲基丙烯酸羟乙酯;
(2)甲基丙烯酸与乙二醇发生酯化反应生成甲基丙烯酸羟乙酯;
(3)乙烯与溴水发生加成反应,再发生水解反应生成乙二醇.
解答 解:(1)甲基丙烯酸羟乙酯含碳碳双键,发生加聚反应生成聚甲基丙烯酸羟乙酯,反应为 ,
,
故答案为: ;
;
(2)甲基丙烯酸与乙二醇发生酯化反应生成甲基丙烯酸羟乙酯,反应为 ,
,
故答案为: ;
;
(3)乙烯与溴水发生加成反应,再发生水解反应生成乙二醇,发生的反应为 ,
,
故答案为: .
.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的结构、官能团、性质为解答的关键,侧重分析与应用能力的考查,注意有机反应的书写,题目难度不大.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:解答题
 NH3可用来制尿素(
NH3可用来制尿素(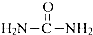 )等化学肥料.
)等化学肥料.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2+2Br-═2Cl-+Br2、Zn+Cu2+═Zn2++Cu均为单质被还原的置换反应 | |
| B. | 2Na2O2+2H2O═4NaOH+O2↑、Cl2+H2O═HCl+HClO均为水作还原剂的氧化还原反应 | |
| C. | Cl元素的单质在化学反应中只表现氧化性 | |
| D. | NaSO3与H2O2的反应为氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是酸性氧化物,能与NaOH溶液反应 | |
| B. | Na2O、Na2O2组成元素相同,与CO2反应产物也相同 | |
| C. | CO2,SO2排放到空气中都能形成酸雨,应严格控制排放 | |
| D. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:5 | B. | 3:1 | C. | 5:1 | D. | 7:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化锰具有还原性,可用于实验室制备氯气 | |
| B. | Na2O2能与水或二氧化碳反应生成氧气,可用作供氧剂 | |
| C. | 碳酸氢钠能与碱反应,可用作食品的膨松剂 | |
| D. | SO2具有漂白性,可用标准KMnO4溶液滴定食品中SO2残留量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com