
在溶液中能大量共存,加入OH-有沉淀析出,加入H+有气体放出的是( )
A.Na+、Cu2+、Cl-、SO42- B.Fe3+、K+、SO42-、NO3-
C.H+、Al3+、OH-、NO3- D.Na+、Ca2+、Cl-、HCO3-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A.第ⅠA族元素的金属性比第ⅡA族元素的金属性强
B.第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
C.同周期非金属氧化物对应的水化物的酸性从左到右依次增强
D.第三周期元素的离子半径从左到右逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
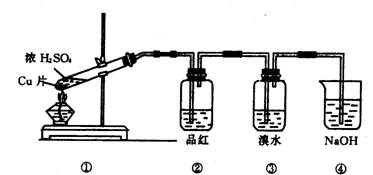
根据下图所示的实验装置,回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式
(2)证明SO2具有漂白性的现象是 ,再加热该溶液,现象是 .
(3)装置③中的现象是 ,证明SO2具有 .
(4)装置④的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应原理在科研和生产中有广泛应用。
(1)利用“化学蒸气转移法”提纯金属钨的反应原理为
该反应在石英真空管中进行,如下图所示:
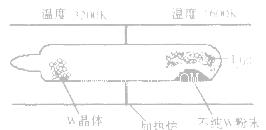
①反应(I)的平衡常数表达式K=_______,若K=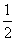 ,向某恒容密闭容器中加入1mol I2(g)和足量W(s),反应达到平衡时I2(g)的转化率为__________。
,向某恒容密闭容器中加入1mol I2(g)和足量W(s),反应达到平衡时I2(g)的转化率为__________。
②反应(I)的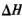 ____0(填“>”或“<”),上述反应体系中可循环使用的物质是_________。
____0(填“>”或“<”),上述反应体系中可循环使用的物质是_________。
③能够说明上述反应已经达到平衡状态的有_________(填序号)。
a.I2与WI2的浓度相等
b.W的质量不再变化
c.容器内混合气体的密度保持不变
d.单位时间内,金属钨消耗的物质的量与碘化钨生成的物质的量相等.
(2)25℃时,NaHSO3的水解平衡常数=1.0×10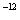 mol
mol ,则该温度下
,则该温度下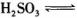
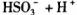 的电离常数
的电离常数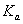 =____mol
=____mol ,若向H2SO3溶液中加入少量的I2,则溶液中
,若向H2SO3溶液中加入少量的I2,则溶液中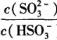 将________(填“增大”、“减小”或“不变”)。
将________(填“增大”、“减小”或“不变”)。
(3)直接排放含SO2的烟气会形成酸雨,危害环境。用Na2SO3溶液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:

当吸收液呈中性时,溶液中离子浓度由大到小的顺序为_________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.摩尔是一种国际基本物理量
B.标准状况下气体摩尔体积约为22.4L
C.1mol氧的质量为16g
D.在同温同压下,相同体积的任何气体单质所含分子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用下列溶质配制一种混合溶液,已知溶液中C(K+)=C(Cl-)=1/2C(Na+)=C(SO42-),则其溶质可能是( )
A.KCl、Na2SO4 B.KCl、Na2SO4、NaCl
C.NaCl、Na2SO4、K2SO4 D.KCl、K2SO4、Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃、101 kPa条件下:4Al(s)+3O2(g)===2Al2O3(s) ΔH=-2834.9 kJ/mol
4Al(s)+2O3(g)===2Al2O3(s) ΔH=-3119.1 kJ/mol,由此得出的结论正确的是( )
A.等质量的O2比O3能量低,由O2变O3为吸热反应
B.等质量的O2比O3能量低,由O2变O3为放热反应
C.O3比O2稳定,由O2变O3为吸热反应 D.O2比O3稳定,由O2变O3为放热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com