
| A. | ①④ | B. | ②③ | C. | ②⑥ | D. | ②③⑥ |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动.使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答 解:A.加入AgNO3溶液后,AgNO3和HBr反应导致平衡正向移动,则溶液颜色变浅,能用平衡移动原理解释,故不选;
②铁在潮湿的空气中易生锈是电化学腐蚀,不是可逆反应,故选;
③增大压强,平衡正向移动,气体颜色变浅,但颜色加深是体积缩小,二氧化氮浓度变大,不能用平衡移动原理解释,故选;
④合成氨反应是放热反应,降低温度平衡正向移动,提高氨的产率,故不选;
⑤K为气体,减小生成物的浓度可使平衡正向移动,能用勒夏特列原理解释,故不选;
⑥反应CO(g)+NO2(g)?CO2(g)+NO(g)(正反应为放热反应),达到化学平衡后,升高温度平衡逆向移动,所以二氧化氮的浓度变大,体系的颜色加深,故不选;
故选B.
点评 本题考查勒夏特列原理知识,题目难度不大,注意勒夏特列原理的使用对象,注意改变压强的本质是改变体积影响反应混合物的浓度.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | N2和H2催化加热制取氨气 | B. | 加热NH4Cl制取氨气 | ||
| C. | 将浓氨水向氧化钙固体上滴加 | D. | 将NH4Cl溶液和NaOH溶液混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(KJ/mol) | 1681 | 1251 | 1140 | 1008 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3Cl+Cl2$\stackrel{光照}{→}$CH2Cl2+HCl | |
| B. | CH2=CH2+HOCl$\stackrel{催化剂}{→}$HOCH2-CH2Cl | |
| C. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| D. | 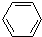 +Br2$\stackrel{催化剂}{→}$ +Br2$\stackrel{催化剂}{→}$ -Br+HBr -Br+HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 阅读下列短文,回答相关问题.
阅读下列短文,回答相关问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化锰和浓盐酸反应:MnO2+4H++4Cl-=Mn2++2Cl2↑+2H2O | |
| B. | 碳酸钡和稀硝酸反应:CO32-+2H+=CO2↑+H2O | |
| C. | 钠和水反应:2Na+2H2O=2 Na++2OH-+H2↑ | |
| D. | 铜和氯化铁溶液反应:Fe3++Cu=Fe2++Cu2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com