
【题目】下列叙述中正确的是( )
A.摩尔是表示物质所含微粒数量以及物质质量的具有双重意义的单位
B.摩尔是国际单位制中7个基本物理量
C.含有6.02×1023个氧原子的H3PO4的物质的量是0.25mol
D.2H既可以表示2个氢原子又可以表示2mol氢原子
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】根据所学知识,完成题目:
(1)在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为(填序号) .
A.9
B.13
C.11~13之间
D.9~11之间
(2)25℃时,向0.1molL﹣1的氨水中加入少量氨化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号) .
A.氨水与氯化铵发生化学反应
B.氯化铵溶液水解显酸性,增加了c(H+)
C.氯化铵溶于水,电离出大量按离子,抑制了氨水的电离,使c(OH)减小
(3)室温下,如果将0.1mol NH4Cl和0.05molNaOH全部溶于水,形成混合溶液(假设无损失)①和两种粒子的物质的量之和等于0.1mol.
②和两种粒子的物质的量之和比OH﹣多0.05mol.
(4)已知某溶液中只存在OH﹣、H+、NH4+、Cl四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:A、c(Cl﹣)>c(NH ![]() )>c(H+)>c(OH﹣)B、c(Cl﹣)>c(NH
)>c(H+)>c(OH﹣)B、c(Cl﹣)>c(NH ![]() )>c(OH+)>c(H+)
)>c(OH+)>c(H+)
C、c(Cl﹣)>c(H+)>c(NH ![]() )>c(OH﹣)D、c(NH
)>c(OH﹣)D、c(NH ![]() )>c(Cl﹣)>c(OH﹣)>c(H+)
)>c(Cl﹣)>c(OH﹣)>c(H+)
①若溶液中只溶解了一种溶质,该溶质是 , 上述离子浓度大小顺序关系中正确的是(选填序号) .
②若上述关系中C是正确的,则溶液中溶质的化学式是 .
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)(填“>”、“<”或“=”,下同)c(NH3H2O),混合后溶液中c(NH ![]() )与c(Cl﹣)的关系:c(NH
)与c(Cl﹣)的关系:c(NH ![]() )c(Cl﹣).
)c(Cl﹣).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙酸和乙醇的叙述不正确的是( )
A. 它们都是烃的衍生物B. 它们分子中都含有羟基
C. 它们的官能团不同D. 它们具有相同的化学特性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是()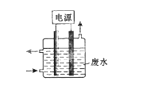
A.用石墨作阳极,铁作阴极
B.阳极的电极反应式为:Cl-+2OH--2e-=ClO-+H2O
C.阴极的电极反应式为:2H2O+2e-=H2↑+2OH-
D.除去CN-的反应:2CN-+5ClO-+2H+=N2↑+2CO2↑+5Cl-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2015·上海)研究电化学腐蚀及防护的装置如右图所示。下列有关说法错误的是( )
A.d为石墨,铁片腐蚀加快
B.d为石墨,石墨上电极反应为:O2 + 2H2O + 4e → 4OH–
C.d为锌块,铁片不易被腐蚀
D.d为锌块,铁片上电极反应为:2H+ + 2e → H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废铅蓄电池量急速增加所引起的铅污染日益严重.工业上从废铅蓄电池的铅膏中回收铅的工艺流程如图 
(1)铅蓄电池的总反应为Pb+PbO2+2H2SO4═2PbSO4+2H2O,该蓄电池放电时的负极反应式为 , 放电后该电极质量(填“增大”“减小”或“不变”).
(2)步骤①中加入Na2SO3的作用是 .
(3)写出步骤②证明PbCO3沉淀已经洗涤干净的实验操作方法: .
(4)若用NH4HCO3和NH3H2O为脱硫转化剂,也可对上述流程中的含铅渣泥进行处理.图2是NH4HCO3和NH3H2O用量对含铅渣泥中脱硫率的影响:
从图形可以看出,应选择NH4HCO3和NH3H2O用量为理论用量的倍.该条件下步骤③从母液可获得副产品为 .
(5)步骤④使用纯铅和粗铅作电极,PbSiF6作电解质,可进行粗铅精炼.则阳极的电极材料是 , 阴极的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42﹣可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( ) 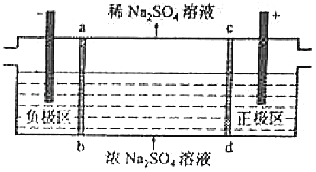
A.通电后中间隔室的SO42﹣离子向正极迁移,正极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.负极反应为2H2O﹣4e﹣=O2+4H+ , 负极区溶液pH降低
D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中氧原子数目与6.8gH2O2中氧原子数目一定相等的是( )
A.6.72L CO
B.6.6gCO2
C.8gSO3
D.9.8gH2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com