
【题目】某pH = l的无色透明溶液中,能大量共存的是
A. Na+、NO3-、I- B. K+、AlO2-、Cl-
C. Cu2+、SO42-、NO3- D. NH4+、SO42-、Br-
科目:高中化学 来源: 题型:
【题目】常温下,一定浓度的某酸HA溶液的pH=5,下列有关说正确的是
A. 向溶液中加入适量NaA固体,若溶液pH不变,则HA为强酸
B. 若HA为弱酸,则该溶液导电能力比等体积pH=5的盐酸弱得多
C. 若HA为弱酸,则加入等体积pH=9的NaOH溶液,所得溶液pH>7
D. 取该溶液1.00mL,加水稀释至1000mL,所得溶液pH=8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池具有广阔的发展前途,科学家近年研制出一种微型的燃料电池,采用甲醇取代氢气做燃料可以简化电池设计,该电池有望取代传统电池.某学生在实验室利用碱性甲醇燃料电池电解Na2SO4溶液.
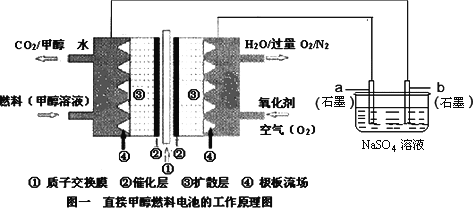
请根据图示回答下列问题:
(1)图中a电极是_____________(填“正极”、“负极”、“阴极”或“阳极”).该电极上发生的电极反应式为__________________.
(2)碱性条件下,通入甲醇的一极发生的电极反应式为________________.
(3)当消耗3.36 L氧气时(已折合为标准状况),理论上电解Na2SO4溶液生成气体的总物质的量是____________mol.
(4)若a、b电极材料分别为铁和石墨,则电解总反应化学方程式为____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取0.3 mol/L HY溶液与0.3 mol/L NaOH溶液等体积混合(不计混合后溶液体积变化),测得混合溶液的pH=9,则下列说法(或关系式)正确的是
A. 混合溶液中由水电离出来的c(OH-)=1×10-9 mol/L
B. 混合溶液中离子浓度大小次序为:c(Y-)>c(Na+)>c(OH-)>c(H+)
C. c(OH-)-c(HY)=c(H+)=1×10-9 mol/L
D. c(Na+)=c(Y-)+c(HY)="0.3" mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.减少交通事故除遵守交通法规正确驾驶外,安全措施也极为重要。汽车的安全气嚢内有叠氮化钠(NaN3)与硝酸铵(NH4NO3)等物质。当汽车在高速行驶中受到猛烈撞击时,这些物质会迅速发生分解反应,产生大量气体,充满气囊,从而保护驾驶员和乘客的安全。
请回答下列问题:
(1)下列判断正确的是_______
A.道路起雾与H2O分子的化学键断裂有关
B.NH4NO3中只含有极性共价键
C.NaN3受到猛烈撞击时化学键一定断裂
D.NaN3、NH4NO3均属于离子化合物
(2)汽车的安全气囊内叠氮化钠爆炸过程中的能量变化如图所示:
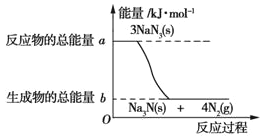
①叠氮化钠的爆炸反应属于_______(填“吸热”或“放热”)反应。
②若爆炸过程中有18mol 非极性键生成(一个共用电子对为一个化学健),则反应的能量变化为______kJ,消耗叠氮化钠的质量为_________g。
③若安全气嚢的体积为VL,NaN3的爆炸在ts内完成,反应过程中消耗292.5g NaN3,则用N2表示的反应速率为____________。
II.(3)已知X、Y、Z、W分别是元素周期表中的短周期元素,且原子序数依次增大。X、W为同主族元素,Y、Z为同周期的相邻元素。W原子的质子数等子Y、Z原子的最外层电子数之和。Y与X形成的分子中含有3个共价键,X、Y、Z所形成的常见化合物是汽车安全气囊中的一种填充物。请回答下列问题:
①写出X、Y、W形成化合物的电子式___________。
②一定温度下,X2、Y2在容积为5L的密闭容器中发生可逆反应,充入的X2和Y2的物质的量分别是6mol和3mol,达到化学平衡状态时生成物的物质的量为2.4mol。达到化学平衡状态时,混合气体中Y2的体积分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下CH3COOH的电离常数K=1.6×10-5。该温度下,向20ml 0.01mol/L CH3COOH溶液在逐滴加入0.01mol/L KOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:

(1)a点溶液中c(H+)为 ,pH约为 。
(2) a、b、c、d四点中水的电离程度最大的是 点,滴定过程中宜选用 作指示剂,滴定终点在 (填“c点以上”或“c点以下”)。
(3)下列操作中可能使所测CH3COOH溶液的浓度数值偏低的是 (填字母)。
A.酸式滴定管未用待测溶液润洗
B.锥形瓶用待测溶液润洗
C.放出酸液的滴定管开始有气泡,放出液体后气泡消失
D.碱式滴定管滴定前有气泡,滴定终点时气泡消失
E.碱式滴定管滴定前读数正确,滴定后俯视读数
(4)若向20ml稀氨水中逐滴加入等浓度的盐酸,下列变化趋势正确的是 (填序号).

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]俗称莫尔盐,是浅绿色晶体,可溶于水,在100℃~110℃时分解,常用作定量分析中的标准试剂。某化学小组以废铁屑为原料在实验室中进行实验探究——制备硫酸亚铁铵并检验其纯度,过程如下:
I.制备硫酸亚铁铵
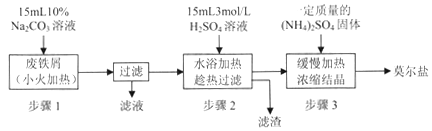
请回答下列问题:
(1)步骤l的作用是_________。(用离子方程式及必要的文字说明);
(2)步骤2中所加硫酸需过量,且不宜等到铁屑完全反应后才过滤,其中蕴含的道理是_______________;
II.测定硫酸亚铁铵的纯度
称取mg实验室制备的硫酸亚铁铵样品,配成500ml溶液,取25. 00mL硫酸亚铁按溶液,用0 . 1mol/L的酸性KMnO4溶液进行滴定,再重复滴定两次。
(3)配制(NH4)2SO4·FeSO4溶液所用的蒸馏水,通常需加热煮沸一段时间后,冷却至室温再使用,这样操作的好处是___________________;
(4)滴定时发生反应的离子方程式为___________________;
(5)滴定终点时的现象为 ___________________;
(6)三次滴定测得酸性KMnO4溶液的用量平均值为VmL,则硫酸亚铁铵样品的纯度为__________;
(7)化学小组分析发现这种检测纯度的方法不够准确,目前处理氮氧化物污染的方法有多种,请你帮助他们设计一种检测方案________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com