
【题目】反应 2SO2(g)+O2(g) ![]() 2SO3(g) ΔH<0,若在恒压绝热容器中发生,下列选项表明反应一定已达平衡状态的是
2SO3(g) ΔH<0,若在恒压绝热容器中发生,下列选项表明反应一定已达平衡状态的是
A.容器内的温度不再变化
B.容器内的压强不再变化
C.相同时间内,v(SO2)与 v(SO3)相等
D.容器内气体的浓度 c(SO2)∶c(O2)∶c(SO3)=2∶1∶2
科目:高中化学 来源: 题型:
【题目】已知25 ℃时,AgI饱和溶液中c(Ag+)为1.23×10-8mol·L-1,AgCl的饱和溶液中c(Ag+)为1.25×10-5mol·L-1。若在5 mL含有KCl和KI各为0.01 mol·L-1的溶液中,加入8 mL 0.01 mol·L-1AgNO3溶液,下列叙述正确的是( )
A.混合溶液中c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-)
B.混合溶液中c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-)
C.加入AgNO3溶液时首先生成AgCl沉淀
D.混合溶液中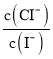 约为1.02×10-3
约为1.02×10-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】玻璃钢可由酚醛树脂和玻璃纤维制成。
(1)酚醛树脂由酚醛和甲醛缩聚而成,反应有大量热放出,为防止温度过高,应向有苯酚的反应釜___________加入甲醛,且反应釜应装有________________装置。
(2)玻璃纤维由玻璃拉丝得到。普通玻璃由石英砂、___________和石灰石(或长石)高温熔融而成,主要反应的化学方程式为______________。
(3)玻璃钢中玻璃纤维的作用是____________。玻璃钢具有__________等优异性能(写出两点即可)
(4)下列处理废旧热固性酚醛塑料的做法合理的是_____________
a.深埋
b.粉碎后用作树脂填料
c.用作燃料
d.用有机溶剂将其溶解,回收树脂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究卤代烃的化学性质,某化学课外小组的学生进行了如下实验。
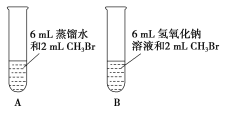
(1)甲同学设计了A、B两个实验,充分振荡反应后,甲先从试管A的水层中取出少量溶液,滴入盛装有硝酸酸化的硝酸银溶液的试管中,观察到的实验现象是____;后从试管B(NaOH溶液的浓度是0.5 mol·L-1)的水层中取出少许溶液,滴入盛有足量硝酸酸化的硝酸银溶液的试管中,观察到的实验现象是____,写出该反应的化学方程式:____。A、B两个实验说明____。
(2)乙同学在B的基础上设计装置C,研究氢氧化钠溶液和CH3Br的反应。浸有乙醇的棉花的作用是____,有人认为,控制装置C中水浴温度是本实验的关键,则应控制水浴温度低于____的沸点。
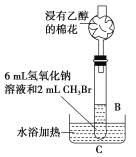
(3)丙同学将NaOH溶液的浓度从0.5 mol·L-1增大到1.0 mol·L-1、1.5 mol·L-1,经过相同的时间(试管中还有油滴)后从试管B的水层中取出少许溶液,滴入盛有足量硝酸酸化的硝酸银溶液的试管中,发现生成沉淀的质量依次增大,该现象说明____,还可以通过其他实验操作说明该结论,简述另一种实验思想:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向0.1mol/LCH3COOH溶液中逐渐加入NaOH固体,恢复至原温度后溶液中的关系如图所示(忽略溶液体积变化)。下列有关叙述不正确的是( )

A.CH3COOH的Ka=1.0×10-4.7
B.C点的溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
C.B点的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH-)
D.A点的溶液中:c(CH3COO-)+c(H+)+c(CH3COOH)-c(OH-)=0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,水的电离达到平衡:H2O![]() H++OH- ΔH>0,下列叙述正确的是( )
H++OH- ΔH>0,下列叙述正确的是( )
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H﹢)增大,Kw不变
C.向水中通入少量HCl气体,平衡正向移动,c(H﹢)增大
D.将水加热,Kw增大,pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: (1)Fe2O3(s)+![]() C(s)=
C(s)=![]() CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
![]() 则
则![]() 的ΔH是( )
的ΔH是( )
A.-824.4 kJmol-1B.-627.6kJmol-1C.-744.7kJmol-1D.-169.4kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以熔融的碳酸盐(K2CO3)为电解液,泡沫镍为电极,氧化纤维布为隔膜(仅允许阴离子通过)可构成直接碳燃料电池,其结构如图所示,下列说法正确的是
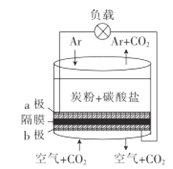
A.该电池工作时,CO32-通过隔膜移动到a极
B.若a极通入空气,负载通过的电流将增大
C.b极的电极反应式为2CO2+O2-4e- =2CO32-
D.为使电池持续工作,理论上需要补充K2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=QkJ·mol1(Q>0)。下列说法正确的是( )
2SO3(g) ΔH=QkJ·mol1(Q>0)。下列说法正确的是( )
A.相同条件下,2molSO2(g)和1molO2(g)所具有的能量小于2molSO3(g)所具有的能量
B.将2molSO2(g)和1molO2(g)置于一密闭容器中充分反应后,放出热量为QkJ
C.对于指定可逆反应的ΔH,表示达到平衡状态时的热量变化
D.如一定量SO2(g)和O2(g)置于某密闭容器中充分反应放热QkJ,则此过程中2molSO2(g)被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com