
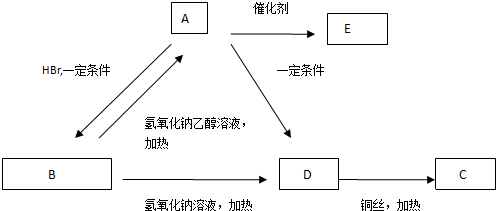
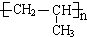 ,A与HBr发生加成反应生成B,B为卤代烃,B的核磁共振氢谱图上有3个吸收峰,则B为BrCH2CH2CH3,B在氢氧化钠醇溶液、加热条件下发生消去反应生成丙烯,B在氢氧化钠水溶液、加热条件下发生水解反应生成D为CH3CH2CH2OH,D发生催化氧化生成C为CH3CH2CHO,丙烯在一定条件下与是发生反应生成CH3CH2CH2OH,据此解答.
,A与HBr发生加成反应生成B,B为卤代烃,B的核磁共振氢谱图上有3个吸收峰,则B为BrCH2CH2CH3,B在氢氧化钠醇溶液、加热条件下发生消去反应生成丙烯,B在氢氧化钠水溶液、加热条件下发生水解反应生成D为CH3CH2CH2OH,D发生催化氧化生成C为CH3CH2CHO,丙烯在一定条件下与是发生反应生成CH3CH2CH2OH,据此解答.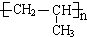 ,A与HBr发生加成反应生成B,B为卤代烃,B的核磁共振氢谱图上有3个吸收峰,则B为BrCH2CH2CH3,B在氢氧化钠醇溶液、加热条件下发生消去反应生成丙烯,B在氢氧化钠水溶液、加热条件下发生水解反应生成D为CH3CH2CH2OH,D发生催化氧化生成C为CH3CH2CHO,丙烯在一定条件下与是发生反应生成CH3CH2CH2OH,
,A与HBr发生加成反应生成B,B为卤代烃,B的核磁共振氢谱图上有3个吸收峰,则B为BrCH2CH2CH3,B在氢氧化钠醇溶液、加热条件下发生消去反应生成丙烯,B在氢氧化钠水溶液、加热条件下发生水解反应生成D为CH3CH2CH2OH,D发生催化氧化生成C为CH3CH2CHO,丙烯在一定条件下与是发生反应生成CH3CH2CH2OH,| 水 |
| △ |
| 催化剂 |
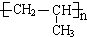 ,
,| 醇 |
| △ |
| 水 |
| △ |
| 催化剂 |
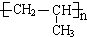 ;BrCH2CH2CH3+NaOH
;BrCH2CH2CH3+NaOH| 醇 |
| △ |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
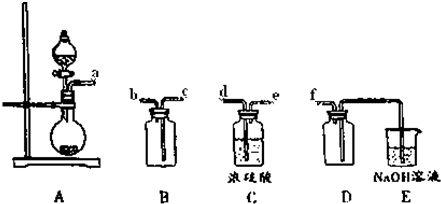
| A、[N(CH3)4]+中只含共价键 |
| B、该反应中,SO2作氧化剂 |
| C、SO2漂白品红是利用其强氧化性 |
| D、每吸收标准状况下的SO211.2L,生成15.4g[N(CH3)4]2 S2O6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 .现有A、B、C、D、E、F六种有机物有如下转化,其中A的分子式为C4H8O3.下列判断正确的是( )
.现有A、B、C、D、E、F六种有机物有如下转化,其中A的分子式为C4H8O3.下列判断正确的是( )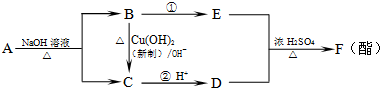
| A、有机物A结构可能有四种 |
| B、反应①属于氧化反应 |
| C、有机物B、D的最简式相同 |
| D、有机物E是交警检测酒驾的重要物证 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不同类的有机物可以有相同的官能团 |
| B、醚类的官能团是醚键 |
| C、所有的烷烃和芳香烃都没有官能团 |
| D、同一有机物可以含不同种官能团 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com