
| A. | 9g | B. | 18g | C. | 22g | D. | 44g |
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 维生素C难溶于水 | |
| B. | 食品中添加维生素C不利于身体健康 | |
| C. | 维生素C具有还原性 | |
| D. | 含维生素C的食物不宜在高温下烹调 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入适量盐酸 | B. | 加入NaOH溶液 | ||
| C. | 置于坩埚中加热 | D. | 配成溶液后通入CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
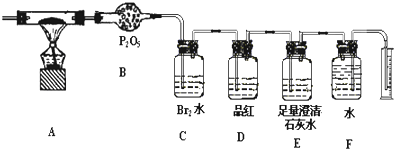
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
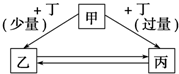 甲、乙、丙、丁均为中学化学中常见的物质,它们之间存在如图所示的转化关系(部分产物略去),甲不可能是( )
甲、乙、丙、丁均为中学化学中常见的物质,它们之间存在如图所示的转化关系(部分产物略去),甲不可能是( )| A. | NaOH溶液 | B. | Fe | C. | Al2O3 | D. | C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是常见原电池装置,电流表G发生偏转:
如图是常见原电池装置,电流表G发生偏转:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com