
【题目】为了检验淀粉水解产物,某学生设计了如下实验方案:
淀粉液![]() 水解液
水解液![]() 混合液
混合液![]() 红色沉淀
红色沉淀
回答下列问题:
(1)试剂1是________,作用是___________________________。
(2)试剂2是________,作用是___________________________。
如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的________(填“能”或“不能”)。
【答案】稀硫酸 催化作用 NaOH溶液 中和H2SO4 不能
【解析】
淀粉在酸或酶的催化下水解,生成葡萄糖。葡萄糖分子中含有醛基,可与新制Cu(OH)2悬浊液发生反应,生成砖红色沉淀Cu2O。分析实验过程可知,过程①为淀粉水解过程,过程③为葡萄糖与新制Cu(OH)2悬浊液发生反应生成砖红色沉淀Cu2O的过程,据此进行分析。
(1)由题给信息可知,淀粉液在试剂1、加热条件下生成水解液,可知该过程为淀粉水解过程,由淀粉水解条件可知,试剂1为稀硫酸,作用是催化淀粉的水解。答案为:稀硫酸;催化作用;
(2)葡萄糖与新制Cu(OH)2悬浊液发生反应的环境应为碱性环境,而过程①中淀粉水解时加入稀硫酸,使得水解液呈酸性环境,则过程②为将酸性环境转化为碱性环境的过程,故试剂2为NaOH溶液,用于中和水解液中的稀硫酸。若实验中没有加入NaOH溶液,则在酸性环境下无法实现实验目的。答案为:NaOH溶液;中和稀硫酸;不能。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列关于周期表的说法正确的是( )
A.C和Si属于第ⅣA族元素,SiH4比CH4稳定
B.N和B属于第二周期元素,原子半径:N>B
C.S和Cl属于第三周期元素,其含氧酸的酸性:H2SO4<HClO3
D.某元素氢化物的化学式为RH3,则其最高价氧化物的水化物可能为HRO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备甲基丙烯酸甲酯的反应装置示意图和有关信息如下:
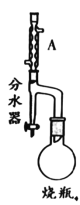
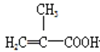 +CH3OH
+CH3OH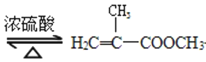 +H2O
+H2O
药品 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度(gcm-3) |
甲醇 | 32 | -98 | -64.5 | 与水混溶,易溶于有机溶剂 | 0.79 |
甲基丙烯酸 | 86 | 15 | 161 | 溶于热水,易溶于有机剂 | 1.01 |
甲基丙烯酸甲酯 | 100 | -48 | 100 | 微溶于水,易溶于有机溶剂 | 0.944 |
已知甲基丙烯酸甲酯受热易聚合;甲基丙烯酸甲酯在盐溶液中溶解度较小;CaCl2可与醇结合形成复合物;
实验步骤:
①向100mL烧瓶中依次加入:15mL甲基丙烯酸、2粒沸石、10mL无水甲醇、适量的浓硫酸;
②在分水器中预先加入水,使水面略低于分水器的支管口,通入冷凝水,缓慢加热 烧瓶。在反应过程中,通过分水器下部的旋塞分出生成的水,保持分水器中水层液面的高度不变,使油层尽量回到圆底烧瓶中;
③当 ,停止加热;
④冷却后用试剂 X 洗涤烧瓶中的混合溶液并分离;
⑤取有机层混合液蒸馏,得到较纯净的甲基丙烯酸甲酯。请回答下列问题:
(1)A装置的名称是_____。
(2)请将步骤③填完整____。
(3)上述实验可能生成的副产物结构简式为_____(填两种)。
(4)下列说法正确的是______
A.在该实验中,浓硫酸是催化剂和脱水剂
B.酯化反应中若生成的酯的密度比水大,不能用分水器提高反应物的转化率
C.洗涤剂X是一组试剂,产物要依次用饱和Na2CO3、饱和CaCl2溶液洗涤
D.为了提高蒸馏速度,最后一步蒸馏可采用减压蒸馏;该步骤一定不能用常压蒸馏
5)实验结束收集分水器分离出的水,并测得质量为2.70g,计算甲基丙烯酸甲酯的产率约为_____。实验中甲基丙烯酸甲酯的实际产率总是小于此计算值,其原因不可能是_____。
A.分水器收集的水里含甲基丙烯酸甲酯
B.实验条件下发生副反应
C.产品精制时收集部分低沸点物质
D.产品在洗涤、蒸发过程中有损失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.钢铁发生电化学腐蚀时,正极上发生的反应为 Fe-2e-=Fe2+
B.用惰性电极分别电解熔融的NaCl和饱和食盐水时,阳极的电极反应式均为:2Cl- -2e-=Cl2↑
C.铜锌原电池工作时,若有13 克锌被溶解,外电路就有0.2 mol电子通过
D.电解精炼铜时,粗铜作阳极,纯铜作阴极,硫酸铜溶液作电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请用符号表示下列核素或同位素。
(1)质子数为![]() ,中子数为
,中子数为![]() 的
的![]() 原子:______。
原子:______。
(2)质子数和中子数都为9的氟原子:______。
(3)中子数为2的氢原子:______。
(4)中子数分别为8、9、10的氧原子:______。
(5)质量数分别为35、37的氯原子: ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是学习和研究化学的基础。某课外兴趣小组设计了下列装置,验证二氧化碳与过氧化钠反应时需要有水存在。
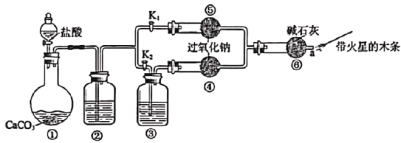
回答下列问题:
I.二氧化碳的制备及纯化:
(1)装置①中反应的离子方程式是___。
(2)装置②中的试剂是___;装置③中的试剂是___。
II.实验验证:
步骤1:打开阀门K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开阀门K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(3)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是___。
(4)过氧化钠与二氧化碳反应的化学方程式为___。
III.实验反思:
(5)有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠与二氧化碳发生了化学反应。”其理由是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,它可以发生反应的类型有( )
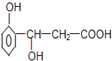
①加成 ②消去 ③水解 ④酯化 ⑤氧化 ⑥加聚
A. ①②③④B. ①②④⑤
C. ①②⑤⑥D. ③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为实验室制取少量乙酸乙酯的装置图。下列关于该实验的叙述中,不正确的是( )

A.向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸
B.试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象
C.实验时加热试管a的目的是及时将乙酸乙酯蒸出并加快反应速率
D.试管b中Na2CO3的作用是除去随乙酸乙酯蒸出的少量乙酸和乙醇,降低乙酸乙酯在溶液中的溶解度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com