
【题目】如图是两组物质之间在一定的条件下相互转化的过程。下列是绿色植物通过光合作用的图示,则说法不正确的是

A.物质X是氧气
B.绿色植物的光合作用属于化学变化
C.C6H12O6属于非电解质
D.C6H12O6与X反应生成二氧化碳和水属于置换反应
科目:高中化学 来源: 题型:
【题目】三盐基硫酸铅(3PbO·PbSO4·H2O,不溶于水)主要适用于不透明的聚氯乙烯硬质管、注射成型制品,也可用于人造革等软质制品。以铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如图所示。

已知:Ksp(PbSO4)=1.82×10-8,Ksp (PbCO3)=1.46×10-13
请回答下列问题:
(1)加入碳酸钠溶液后PbSO4转化为PbCO3。转化的方程式为:PbSO4(s)+CO32-(aq)=PbCO3(s)+SO42-(aq),通过计算(保留2位有效数字)说明该反应程度很大的原因:___________。这一步骤中,也可以将碳酸钠溶液改为碳酸氢钠溶液,写出用碳酸氢钠溶液时的离子方程式:___________。
(2)根据图溶解度曲线(g/100g水),由滤液I得到Na2SO4固体的操作为将“滤液1”___________、___________、用乙醇洗涤后于燥。

(3)步骤③“酸溶”,为提高酸溶速率,可采取的措施是___________(任意写出一条),生成NO的离子方程式:___________。
(4)“滤液2”中可循环利用的溶质为___________(填化学式)。
步骤④“沉铅”时若将Pb(NO3)2溶液与0.02mol·L-1的H2SO4等体积混合生成PbSO4沉淀时,所需Pb(NO3)2溶液的最小物质的量浓度为___________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业采用氯化铵焙烧菱锰矿制备高纯碳酸锰的流程如图所示:

已知:①菱锰矿的主要成分是MnCO3,其余为Fe、Ca、Mg、Al等元素。
②部分阳离子沉淀时溶液的pH:
离子 | Al3+ | Fe3+ | Ca2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 4.1 | 2.2 | 10.6 | 8.1 | 9.1 |
沉淀完全的pH | 4.7 | 3.2 | 13.1 | 10.1 | 11.1 |
③焙烧过程中主要反应为MnCO3+2NH4Cl![]() MnCl2+2NH3↑+CO2↑+H2O。
MnCl2+2NH3↑+CO2↑+H2O。
(1)结合如图1、2、3,分析焙烧过程中最佳的焙烧温度、焙烧时间、![]() 分别为___、___、___。
分别为___、___、___。
|
|
|
如图1焙烧温度对锰浸出率的影响 | 如图2焙烧时间与锰浸出率的关系 | 如图3氯化铵与菱锰矿粉质量比对锰浸出率的影响 |
(2)对浸出液净化除杂时,需先加入MnO2,作用是____,再调节溶液pH的范围为___,将Fe3+和Al3+变为沉淀而除去,然后加入NH4F将Ca2+、Mg2+变为氟化物沉淀除去。
(3)上述流程中可循环使用的物质是_____(填化学式)。
(4)现用滴定法测定产品中锰的含量。实验步骤:称取4.000g试样,向其中加入稍过量的磷酸和硝酸,加热使产品中的MnCO2完全转化为[Mn(PO4)2]3-(其中NO3-转化为NO2-);加入稍过量的硫酸铵,发生反应NO2-+NH4+═N2↑+2H2O以除去NO2-;加入稀硫酸酸化,用60.00mL0.50mol·L-1硫酸亚铁铵标准溶液进行滴定,发生的反应为[Mn(PO4)2]3-+Fe2+═Mn2++Fe3++2PO43-,用5.00mL0.50mol·L-1酸性K2Cr2O7溶液恰好除去过量的Fe2+。
①酸性K2Cr2O7溶液与Fe2+反应的离子方程式为_______。
②试样中锰的质量分数为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体积为1 mL、浓度均为0.10 mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是

A. XOH是弱碱
B. pH=10的两种溶液中的c(X+):XOH大于X2CO3
C. 已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2
D. 当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则c(HCO3-)/c(CO32-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在常温下测得浓度均为0.1molL﹣1的下列四种溶液的pH如下表:
溶质 | NaHCO3 | Na2CO3 | NaF | NaClO |
pH | 8.4 | 11.6 | 7.5 | 9.7 |
(1)用离子方程式表示NaClO溶液的pH = 9.7的原因___________________________。
(2)根据盐溶液的pH,可知①Ka(HClO) ②Ka1(H2CO3) ③Ka(HF) ④Ka2(H2CO3)的由大到小顺序为_________________________________ (填序号)。
(3)将少量CO2通入NaClO溶液中,写出该反应的离子方程式:________________。
(4)常温下,将CO2通入0.1molL﹣1的Na2CO3溶液中至中性,则溶液中2c(CO32-)+ c(HCO3-)=_________________(列计算式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]俗称摩尔盐.硫酸亚铁在空气中易被氧化,但与硫酸铵反应生成摩尔盐后较稳定.模拟工业制备硫酸亚铁铵晶体的实验装置如图所示.回答下列问题:

(1)先用饱和碳酸钠溶液煮沸铁屑(含少量油污、铁锈等),再用清水洗净.用饱和碳酸钠溶液煮沸的目的是________________.仪器a的名称是______________.
(2)按如图连接好装置,经检验气密性良好后加入相应的药品,打开K1、K2,关闭K3,装置B中发生反应的离子方程式可能_______________(填字母序号).
A.Fe+2H+=Fe2++H2↑ B.2Fe+6H+=2Fe3++3H2↑
C. Fe2 03+6H+=2Fe3+ +3H2O D. 2Fe3++Fe=3Fe2+
铁屑快反应完时,打开____________,关闭____________,装置B中的溶液会流入装置A,其原因是_____________________.
(3)常温下,将反应后的溶液放置一段时间,瓶底将结晶析出硫酸亚铁铵.为了测定晶体中Fe2+的含量,称取一份质量为4.0g的硫酸亚铁铵晶体样品,配成溶液.用0.1mol·L-1酸性KMnO4溶液滴定至终点,消耗KMnO4溶液体积为20.00mL.反应到达滴定终点的现象为_________________,计算晶体中Fe2+的质量分数为_________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常温条件下甲、乙、丙三种溶液,甲为0.1 mol·L-1的NaOH溶液,乙为0.1 mol·L-1的盐酸,丙为未知浓度的FeCl2溶液,试回答下列问题:
(1)甲溶液的pH=________。
(2)甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为________。
(3)某化学兴趣小组认为在隔绝空气的环境中,用酸性KMnO4溶液能测定丙溶液的浓度(已知:5Fe2++MnO+8H+===5Fe3++Mn2++4H2O)。
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需________(填写仪器名称)。
②滴定实验要用到酸式滴定管或碱式滴定管,使用该仪器的第一步操作是_______。
③某同学设计的下列滴定方式中,最合理的是________(夹持部分略去,填字母序号),达到滴定终点的现象是__________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Li和石墨的复合材料以及纳米Fe2O3材料作电极的锂离子电池,在循环充放电过程中可实现对磁性的可逆调控(如图)。下列有关说法一定错误的是
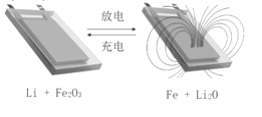
A. 该电池的电解质溶液可以是硫酸溶液
B. 放电时,总反应式是6Li+Fe2O3=3Li2O+2Fe
C. 充电时,阳极的电极反应是2Fe+3Li2O-6e-= Fe2O3+6Li+
D. 充放电过程中,电池可在被磁铁不吸引和吸引之间循环调控
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com