
(10分) 已知X、Y、Z是阳离子,K是阴离子,M、N是分子。它们都由短周期元素组成,且具有以下结构特征和性质:
①它们的核外电子总数都相同;
②N溶于M中,滴入酚酞,溶液变红;
③Y和K都由A.B两元素组成,Y核内质子数比K多2个;
④X和N都由A、C两元素组成,X和Y核内质子总数相等;
⑤X和K的浓溶液在加热条件下生成M和N;
⑥Z为单核离子,向含有Z的溶液中加入少量含K的溶液,有白色沉淀生成,再加入过量的含K或Y的溶液,沉淀消失。
回答下列问题:
(1)Y的化学式为 ;N的电子式为
(2)试比较M和N的稳定性:M (填“>”或“<”)N。
(3)写出Z和N的水溶液反应的离子方程式: ;
(4))上述六种微粒中的两种可与硫酸根形成一种含三种离子的盐,向该盐的浓溶液中逐滴加入0.1 的NaOH溶液,出现了如图中a、b、c三个阶段的图像,
的NaOH溶液,出现了如图中a、b、c三个阶段的图像,
①写出b阶段的离子方程式:
②根据图像判断该盐的化学式为 。

(9分)(1)H3O+
(1分) 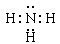 (1分)(2)> (1分)
(1分)(2)> (1分)
(3) Al3++3NH3·H2O = Al(OH)3↓+3NH4+ (2分)
(4)①NH4++OH-= NH3·H2O (2分) ②NH4Al(SO4)2 (2分)
【解析】
试题分析:N溶于M中,滴入酚酞,溶液变红,则N应该是氨气,M是水。X和K的浓溶液在加热条件下生成M和N,所以X和K分别是NH4+和OH-。Y和K都由A、B两元素组成,Y核内质子数比K多2个,所以Y是H3O+;Z为单核离子,向含有Z的溶液中加入少量含K的溶液,有白色沉淀生成,再加入过量的含K或Y的溶液,沉淀消失,所以Z是 Al3+。
(1)Y的化学式为H3O+;氨气是共价化合物,电子式为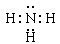 。
。
(2)非金属性越强,氢化物的稳定性越强,氧元素的非金属性强于氮元素的,所以水的稳定性强于氨气的。
(3)氢氧化铝是两性氧化物,但不能溶于氨水中,所以该反应的方程式是 Al3++3NH3·H2O =Al(OH)3↓+3NH4+。
(4)根据图像可知,产生的沉淀应该是氢氧化铝。又因为中间一段沉淀是不变的,这说明还含有NH4+,所以b阶段的离子方程式是NH4++OH-= NH3·H2O;根据微粒的电荷数可知,该盐的化学式是NH4Al(SO4)2 。
考点:考查物质的性质、转化以及方程式的书写的鞥
点评:本题主要是以常见微粒的结构和性质,综合考查学生对基础知识的掌握程度以及灵活运用知识解决实际问题的能力。


科目:高中化学 来源: 题型:
(分)已知X、Y、Z、W四种短周期主族元素,原子半径X>Y>Z>W,X、Y、Z处于同一周期,Z、W处于同一主族,X、Y、Z原子序数之和为40,最外层电子数之和为10。据此回答下列有关问题:
⑴X、Y、Z处于____________周期。
⑵若Z原子最外电子数是Y原子最外层电子数的2倍。则元素Y的最高价氧化物对应水化物在水中的电离方程式为_______________;X和W形成的化合物XW2的电子式为________。
⑶若X、W能形成1:1型离子化合物,则其水溶液呈_______性(填“中”、“酸”、“碱”),
并写出电解YZ2溶液的化学方程式___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(共10分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,反应方程式为2NH3+3CuO
![]() N2+3H2O+3Cu,用示意图中的装置可以实现该反应。回答下列问题:
N2+3H2O+3Cu,用示意图中的装置可以实现该反应。回答下列问题:
(1)A中发生反应的化学方程式是 。检验氨气通常采用的方法及现象是_________ ____________, 。
(2)B中加入的物质是 ,其作用是 。
(3)实验时C中观察到的现象是 ,该反应中氨的作用是_______剂。
(4)若要检验反应生成的水,可将试管D及烧杯部分改成两个相连的干燥管,第一个干燥管X内装有_____________,现象是___________________;第二个干燥管Y内装有碱石灰,作用是____________________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河北省衡水中学高一下学期一调考试化学试卷(带解析) 题型:实验题
(共10分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,反应方程式为2NH3+3CuO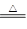 N2+3H2O+3Cu,用示意图中的装置可以实现该反应。回答下列问题:
N2+3H2O+3Cu,用示意图中的装置可以实现该反应。回答下列问题:
(1)A中发生反应的化学方程式是 。检验氨气通常采用的方法及现象是_________ ______, 。
(2)B中加入的物质是 ,其作用是 。
(3)实验时C中观察到的现象是 ,该反应中氨的作用是_______剂。
(4)若要检验反应生成的水,可将试管D及烧杯部分改成两个相连的干燥管,第一个干燥管X内装有_____________,现象是___________________;第二个干燥管Y内装有碱石灰,作用是____________________________。
查看答案和解析>>
科目:高中化学 来源:2014届河北省高一下学期一调考试化学试卷(解析版) 题型:实验题
(共10分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,反应方程式为2NH3+3CuO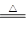 N2+3H2O+3Cu,用示意图中的装置可以实现该反应。回答下列问题:
N2+3H2O+3Cu,用示意图中的装置可以实现该反应。回答下列问题:

(1)A中发生反应的化学方程式是 。检验氨气通常采用的方法及现象是_________ ______, 。
(2)B中加入的物质是 ,其作用是 。
(3)实验时C中观察到的现象是 ,该反应中氨的作用是_______剂。
(4)若要检验反应生成的水,可将试管D及烧杯部分改成两个相连的干燥管,第一个干燥管X内装有_____________,现象是___________________;第二个干燥管Y内装有碱石灰,作用是____________________________。
查看答案和解析>>
科目:高中化学 来源:2014届安徽省高一上学期期末考试化学试卷 题型:填空题
(10分)(1)已知下列变化过程中,0.2 mol R2O72-与0.2 mol K2SO3恰好反应,则R被还原的价态为____。
(2)在100 mL 0.100 mol·L-1的FeBr2溶液中通入Cl2,若要使Fe2+刚好反应完全,则需标准状况下Cl2________ mL。
(3)某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X.
①已知KBrO3在反应中得到电子,则该反应的还原剂是______________________.
②已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为______________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com