
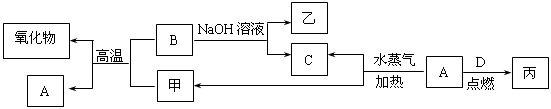
A��B��C��D�����ֳ����ĵ��ʣ�A��BΪ������C��D�����������壬��DΪ����ɫ���塣�ס��ҡ���Ϊ�����Ļ���������ʾ��д��ԡ�����֮������ͼ��ת����ϵ��
 |
��ش��������⣺
��1��B���Ӧ�Ļ�ѧ����ʽ�� ��
B��NaOH��Һ��Ӧ�����ӷ���ʽ�� ��
��������������Һ��Ӧ�����ӷ���ʽ�� ��
��2������B�������ӵ���Һ������Һ��Ӧ�õ�һ�ְ�ɫ�������÷�Ӧ�����ӷ���ʽ��
��
��3��ʵ���Ҽ������Һ���������������ӵIJ���������������
��
��
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����������������������Ҫ��Դ��Ϊ���ƿ��������������ġ����칤�̡��õ���ȫ���֧�֡�
���д�ʩ�����ڡ����칤�̡��������
A���ƹ�ʹ��ȼú������������SO2��Ⱦ
B��ʵʩ�̻����̣������ﳾ��Ⱦ
C�����ƿ���ȼ�ϵ������������������β����Ⱦ
D���Ӵ�ʯ�͡�ú̿�Ŀ����ٶȣ����ӻ�ʯȼ�ϵĹ�Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
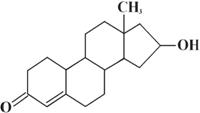
��ŵ�������ڹ��ʰ�ί����ȷ�涨��Υ��ҩƷ�кϳɴ�л�����̴�����ṹ��ʽ��ͼ ��
���й��ڡ�ŵ������˵��������ȷ����
A������ʽ��C18H26O2
B������NaOH����Һ�з�����ȥ��Ӧ
C�����ܷ����ӳɷ�Ӧ��Ҳ�ܷ���������Ӧ
D�����ܷ���������Ӧ��Ҳ�ܷ�����ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����豸����ʱ������ѧ��ת��Ϊ���ܵ���
| A | B | C | D |
|
|
|
|
|
| ��̫���ܵ�� | ����ӵ�� | ̫���ܼ����� | ȼ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������ƣ�Na2S2O3����ϡH2SO4��Һʱ�������·�Ӧ��
Na2S2O3+ H2SO4=Na2 SO4+SO2+S��+H2O ���з�Ӧ����������
A 0.1mol/L Na2S2O3��0.1mol/L H2SO4��Һ��5mL����ˮ5mL����Ӧ�¶�10��
B 0.1mol/L Na2S2O3��0.1mol/L H2SO4��Һ��5mL����ˮ10mL����Ӧ�¶�10��
C 0.1mol/L Na2S2O33��0.1mol/L H2SO4��Һ��5mL����ˮ10mL����Ӧ�¶�30��
D 0.2mol/L Na2S2O3��0.1mol/L H2SO4��Һ��5mL����ˮ10mL����Ӧ�¶�30��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ڻ���ƽ�����װ��ǿ��ԭ���£�N2H4����ǿ��������H2O2���������ǻ��ʱ��������������N2��ˮ���������ų������ȡ���֪0.4molҺ̬�º�����H2O2��Ӧ�����ɵ�����ˮ�������ų�256.65kJ��������
��1��д���÷�Ӧ���Ȼ�ѧ����ʽ__________________________________________��
��2����֪H2O(l)====H2O(g)����H=+44kJ��mol-1����16 gҺ̬��ȼ�����ɵ�����Һ̬ˮʱ���ų���������________kJ��
��3��������ӦӦ���ڻ���ƽ��������ͷŴ������ȺͿ��ٲ������������⣬����һ����ͻ�����ŵ���________________________��
��4����֪ N2(g)+2O2(g)====2 NO2(g)����H=+67.7 kJ��mol-1��
N2H4 (g) ��O2 (g) �� N2(g) ��2H2O (g) ��H = -543kJ/mol
���ݸ�˹����д������NO2��ȫ��Ӧ���ɵ�������̬ˮ���Ȼ�ѧ����ʽ________________________________��
��5����֪�� N2 (g) �� 2O2 (g) �� 2NO2 (g) ��H = + 67.7kJ/mol
N2H4 (g) ��O2 (g) �� N2(g) ��2H2O (g) ��H = -543kJ/mol
1/2H2 (g) �� 1/2F2 (g) �� HF (g) ��H = -269kJ/mol
H2 (g) �� 1/2O2 (g) �� H2O (g) ��H = -242kJ/mol
������Ϊ���÷������������������������Ӧ�ͷ����������ºͷ���Ӧ��
�Ȼ�ѧ����ʽ�� ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ͬ��ͬѹ�£�������������������ռ�е���������ǣ� ��
A��O2 B��CH4 C��CO2 D��SO2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com