
短周期的三种元素X、Y、Z,已知X元素的原子核外只有一个电子,Y元素的原子M层上的电子数是它的内层电子总数的一半,Z元素原子的L层上的电子数比Y元素原子的L层上的电子数少2个,则这三种元素所组成的化合物的化学式不可能是( )
A.X2YZ4 B.XYZ3 C.X3YZ4 D.X4Y2Z7
 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价绝对值相等,Z的核电荷数是Y的2倍,W最外层电子数是最内层电子数的3倍.下列说法正确的是
A.微粒半径:Z2+>W2->R-
B.对应氢化物的稳定性:W>R
C.W与X、W与Z形成的化学物晶体类型相同
D.Y的最高价氧化物对应的水化物是弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
已知浓H2SO4和Fe3+都可以将Cu氧化成Cu2+,浓H2SO4也可以将Br-氧化成Br2,Fe与Br2反应生成FeBr3.由此可以确定上述有关物质氧化性由强到弱的顺序为( )
A.浓H2SO4>Br2>Fe3+>Cu2+ B.浓H2SO4>Cu2+>Fe3+>Br2
C.Br2>浓H2SO4>Fe3+>Cu2+ D.Fe3+>Cu2+>Br2>浓H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为几种晶体或晶胞的示意图:
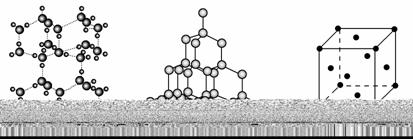
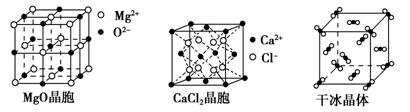
请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是________。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为_______。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能______(填“大于”或“小于”)MgO晶体,原因是_________________。
(4)每个Cu晶胞中实际占有________个Cu原子,CaCl2晶体中Ca2+的配位数为________。
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.Li是最活泼金属,F是最活泼非金属
B.Mg(OH)2碱性比Ca(OH)2强
C.元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行
D.X2+的核外电子数目为18,则X在第四周期第ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应属于加成反应的是( )
A.2CH3CH2OH+2Na—→2CH3CH2ONa+H2↑
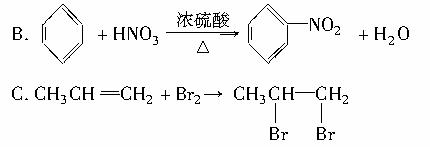
D.CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下将35 mL气态烷烃完全燃烧,恢复到原来状况下,得到二氧化碳气体140 mL,则该烃的分子式为( )
A.C5H12 B.C4H10 C.C3H6 D.C3H8
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应中,不属于离子反应的是( )
A.在水溶液中:CH3COOH+NH3·H2O===CH3COONH4+H2O
B.在水溶液中:Cu(OH)2+2HNO3===Cu(NO3)2+2H2O
C.Fe2O3+3CO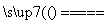 2Fe+3CO2
2Fe+3CO2
D.在水溶液中:CaSO4+Na2CO3===CaCO3↓+Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学研究性学习小组对溶液作如下的归纳总结(均在常温下)。其中正确的是( )
①pH=3的强酸溶液1 mL,加水稀释至100 mL后,溶液pH降低2个单位
②1 L 0.50 mol·L-1 NH4Cl 溶液与2 L 0.25 mol·L-1 NH4Cl 溶液含NH4+ 物质的量前者大
③在某钠盐溶液中含有等物质的量的Cl-、I-、AlO2-、CO32-、NO3-、SiO32-中若干种,当加入过量的盐酸产生气泡,溶液颜色变深,阴离子种数减少3种,则原溶液中一定有CO32-
④pH=4、浓度均为0.1 mol·L-1 的CH3COOH、CH3COONa混合溶液中:
c(CH3COO-)-c(CH3COOH)=2×(10-4-10-10) mol/L
A.①② B.②③ C.①③ D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com