
【题目】下列有关工业生产的叙述中,不正确的是:
A. 电解氧化铝时,用冰晶石降低其熔点 B. 制玻璃时,常加入氧化铁以降低生产成本
C. 添加必要的元素可提高钢材的性能 D. 催化裂化可提高汽油的产量
科目:高中化学 来源: 题型:
【题目】(1)相同物质的量的O2和O3的质量比为_________;所含氧原子的个数比为______________。
(2)2.5 mol Ba(OH)2中含有_________个OH—,2.5 mol Ba(OH)2的质量是____________g。
(3)在标准状况下,1.7 g氨气所占的体积约为__________L,它与标准状况________L硫化氢含有相同数目的氢原子。
(4)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为________________。
(5)同温同压下,SO2与氦气的密度之比为________,若质量相同,两种气体的体积比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH = -92.2kJmol—1,测得0到10秒内,c(H2)减小了0.75molL—1,下列说法正确的是( )
2NH3(g) ΔH = -92.2kJmol—1,测得0到10秒内,c(H2)减小了0.75molL—1,下列说法正确的是( )
A.10到15秒内c(NH3) 增加量等于0.25mol L—1
B.10秒内氨气的平均反应速率为0.025molL—1·s—1
C.达平衡后,分离出少量NH3,v正 增大
D.该反应的逆反应的活化能不小于92.2kJmol—1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早在1807年化学家戴维用电解熔融氢氧化钠制得钠:4NaOH(熔) ![]() 4Na + O2↑+ 2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠:3Fe + 4NaOH
4Na + O2↑+ 2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠:3Fe + 4NaOH ![]() Fe3O4 + 2H2↑ + 4Na↑。下列有关说法正确的是( )
Fe3O4 + 2H2↑ + 4Na↑。下列有关说法正确的是( )

A.电解熔融氢氧化钠制钠,阳极发生电解反应2OH--2e-===H2↑+O2↑
B.盖·吕萨克法制钠原理是利用铁的还原性比钠强
C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数不同
D.目前工业上常用电解熔融氯化钠法制钠(如上图),电解槽中石墨极为阴极,铁为阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在; 钴以Co2O3 ·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中。从废料中回收氧化钴(CoO)的工艺流程如下:

(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为 。
(2)过程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴.则浸出钴的离子反应方程式为(产物中只有一种酸根) 。在实验室模拟工业生产时,也可用盐酸代替酸化的Na2S2O3,但实际工业生产中不用盐酸,请从反应原理分析不用盐酸浸出钴的主要原因 。
(3)用离子方程式表示过程III和IV中Na2CO3的主要作用 。
(4)CoO溶于盐酸可得粉红色的CoCl2溶液.CoCl2含结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2 吸水变色这一性质可制成变色水泥和显隐墨水.图2是粉红色的CoCl2·6H2O晶体受热分解时,剩余固体质量随温度变化的曲线,A物质的化学式是 .

(5)某天然碱的化学式可表示为2Na2CO3·NaHCO3·2H2O,取少量该物质溶于水得稀溶液。下列有关该溶液中微粒的物质的量浓度关系正确的是 (填序号)。
A.c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
B.c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
C.3c(Na+)>5c(CO32-)+5c(HCO3-)
D.将该溶液与少量NaOH溶液混合:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,在玻璃管中放入还原铁粉和石棉绒(成分是硫酸盐材料,是铁粉的载体)的混合物,加热并通入水蒸气,用试管收集产生的经干燥的气体,并靠近酒精灯的火焰。
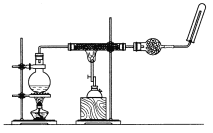
(1)所观察到的现象是_______________,_______________有关反应的方程式是________________。
(2)干燥管内可装入的试剂是________,其作用是________________。干燥管还可用________(装置)代替。
(3)实验开始时应先点燃________,实验结束时,应先熄灭________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与化学反应能量变化相关的叙述正确的是( )
A. 反应物总能量低于生成物总能量时,该反应一定不能发生
B. 化学键的键能越大,物质的能量越高
C. 一个反应的焓变因反应物的用量和反应条件的改变而发生改变
D. 应用盖斯定律,可计算某些难以直接测量的反应焓变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法不正确的是( )

A. 溶液中OH-向电极a移动
B. O2在电极b上发生还原反应
C. 反应消耗的NH3与O2的物质的量之比为4:5
D. 电极a的反应式为2NH3-6e-+6OH-=N2+6H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com