
| A. | 向海带灰浸出液中加入硫酸、双氧水:2I-+2H++H2O2═I2+2H2O | |
| B. | 氯气溶于蒸馏水制氯水:Cl2+H2O?H++Cl-+HClO | |
| C. | 向Al2(SO4)3溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 向沸水中滴加饱和FeCl3制胶体:Fe3++3H2O?Fe (OH)3(胶体)+3H+ |
分析 A.双氧水具.有强的氧化性,能够氧化碘离子;
B.氯气和水反应生成盐酸和次氯酸,次氯酸为弱酸,反应为可逆反应;
C.氢氧化铝是两性氢氧化物,溶液强酸强碱,不溶于弱酸弱碱;
D.向沸水中滴加少量的FeCl3溶液,FeCl3水解生成Fe(OH)3胶体;
解答 解:A.向海带灰浸出液中加入硫酸、双氧水,发生氧化还原反应,离子方程式:2I-+2H++H2O2═I2+2H2O,故A正确;
B.氯气和水反应生成盐酸和次氯酸,次氯酸为弱酸,离子方程式为:Cl2+H2O?H++Cl-+HClO,故B正确;
C.向Al2(SO4)3溶液中加入过量的氨水,反应的离子方程式:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故C错误;
D.向沸水中滴加少量的FeCl3溶液生成氢氧化铁胶体,反应的化学方程式为:FeCl3+3H2O $\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl,其水解方程式为:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3H+,故D正确;
故选C.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意离子方程式书写应遵循客观事实、遵循原子个数、电荷数守恒规律,题目难度中等.


 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电化学腐蚀是造成钢铁腐蚀的主要原因 | |
| B. | 当钢铁表面水膜呈弱酸性或中性时,主要发生吸氧腐蚀正极反应为:O2-4e-+2H2O=4OH- | |
| C. | 在钢铁设施上连接比铁活泼的金属可防止钢铁腐蚀 | |
| D. | 巨型的铁制桥梁一般采用涂油漆的方法来防生锈 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
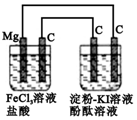
| A. | 电解池中阳极区溶液变红,阴极区溶液变蓝 | |
| B. | 原电池中碳极的电极反应式为:Fe3++e-═Fe2+ | |
| C. | 镁为负极,发生氧化反应 | |
| D. | 电解池中阴极的电极反应式为:2H++e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 它的一氯代物有8种 | |
| B. | 它和丁基苯( )互为同分异构体 )互为同分异构体 | |
| C. | 它的分子中所有的碳原子一定在同一平面上 | |
| D. | 一定条件下,它分别可以发生加成、取代、氧化、消去等反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PbO2是电池的负极 | |
| B. | 正极反应式为:Pb+SO42--2e-═PbSO4 | |
| C. | H2SO4起传导电子的作用 | |
| D. | 电池放电时,溶液pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
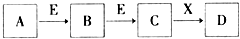 中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )
中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )| A. | 若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁 | |
| B. | 若D为NaOH,则A、B、C均可与X反应生成D | |
| C. | 若D为NaCl,且A可与C反应生成B,则E可能是CO2 | |
| D. | 若D为H2SO4,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应物的总能量大于生成物的总能量的反应一定是吸热反应 | |
| B. | 在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,铜粉仍不溶解 | |
| C. | 铜与稀硝酸反应的离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| D. | 氨气的还原性可以解释氨气与氯化氢的反应实验 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com