
| n |
| V |
| 2 |
| 3 |
| n |
| V |
| 0.5mol |
| 0.5L |
| 2 |
| 3 |
| 2 |
| 3 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;H为气体单质,D为无色气体,D在空气中会出现红棕色,各物质的转化关系如图,(部分反应产物已略去).
已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;H为气体单质,D为无色气体,D在空气中会出现红棕色,各物质的转化关系如图,(部分反应产物已略去).查看答案和解析>>
科目:高中化学 来源: 题型:

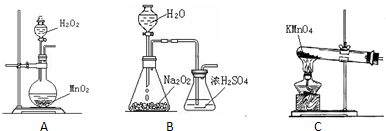
查看答案和解析>>
科目:高中化学 来源: 题型:
 将质量相等的锌片和铜片用导线相连浸入500mL 硫酸铜溶液中构成如下图的装置.(1)此装置为
将质量相等的锌片和铜片用导线相连浸入500mL 硫酸铜溶液中构成如下图的装置.(1)此装置为查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
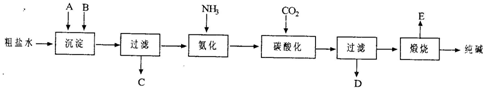
| ||
| ||
| 84(m1-m2) |
| 31m1 |
| 84(m1-m2) |
| 31m1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com