
(14分)用单线桥表示下列反应中电子转移的方向和数目,并填空
(1)2KMnO4 + 16HCl(浓)= 2KCl + 2MnCl2 + 5Cl2↑+ 8H2O
(2)该反应中,元素化合价升高的是 (填元素符号),氧化剂是 还原产物是 氧化性:KMnO4 Cl2(填>、=、<)
(3)反应中若有71克Cl2生成,转移的电子数为 个。
(1)
(2) Cl ; KMnO4; MnCl2 ; > (3)2NA 或 1.024×1024
【解析】
试题分析:(1)氧化还原反应中转移的电子数目=化合价升高的数目=化合价降低的数目,可得:

(2)标化合价,根据化合价的变化可知,该反应中,元素化合价升高的是Cl,氧化剂是KMnO4还原产物是MnCl2,根据氧化剂的氧化性大于氧化产物的氧化性可知:氧化性:KMnO4 > Cl2;
(3)当生成5mol×71g/mol=355g的氯气时,转移的电子为10mol,当生成71克(1mol)Cl2生成,转移的电子为2mol,即2NA个,答案为:2NA;
考点:考查氧化还原反应的中的有关概念和电子转移知识。


科目:高中化学 来源:2014-2015学年湖南省高三上学期第二次月考化学试卷(解析版) 题型:选择题
下表各选项中,不能利用置换反应通过Y得到W的一组化合物是( )
选项化合物 | A | B | C | D |
Y | CO2 | Fe2O3 | SiO2 | FeCl3 |
W | MgO | Al2O3 | CO | CuCl2 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
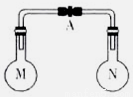
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧
瓶内的气体接触(如图),容器内的压强由大到小的顺序是
编号 | ① | ② | ③ | ④ |
气体M | H2S | H2 | N H3 | NO |
气体N | SO2 | Cl2 | HCl | O2 |
A.①②③④ B.②④①③ C.④①②③ D.①④③②
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省浏阳市高一上第一次月考试卷化学试卷(解析版) 题型:选择题
下列分散系最不稳定的是 ( )
A.向CuSO4溶液中加入Ba(OH)2溶液得到的分散系
B.向水中加入食盐得到的分散系
C.向沸水中滴入饱和FeCl3溶液得到的红褐色液体
D.向NaOH溶液中通入CO2得到的无色溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省浏阳市高一上第一次月考试卷化学试卷(解析版) 题型:选择题
下列实验操作正确的是 ( )
A.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
B.在食盐溶液蒸发结晶的过程中,当蒸发皿中出现较多量固体时即停止加热
C.先在天平两个托盘上各放一张相同质量的纸,再把氢氧化钠固体放在纸上称量
D.过滤时,慢慢地将液体直接倒入过滤器中
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高一上学期期中化学试卷(解析版) 题型:选择题
实现下列变化,一定要加入其它物质作氧化剂的是
A.CaCO3 → CO2 B.NaCl → NaNO3
C.CuO → CuSO4 D.Zn → ZnCl2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高一上学期期中化学试卷(解析版) 题型:选择题
下列萃取和分液结合进行的操作(用煤油为萃取剂从碘水中萃取碘)中,错误的是
A.饱和碘水和煤油加入分液漏斗中后,塞上口部的塞子,且一手压住分液漏斗口部,一手握住活塞部分,把分液漏斗倒转过来用力振荡;
B.静置,待分液漏斗中溶液分层后,先使分液漏斗内外空气相通,以准备放出液体
C.打开分液漏斗的活塞,使全部下层液体沿承接液体的烧杯内壁慢慢流出
D.上层液体在分液漏斗中保存
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高一上学期第一次阶段考试化学试卷(解析版) 题型:填空题
实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
①如图所示的仪器中,配制溶液肯定不需要的是__________________________ (填序号),配制上述溶液还需用到的玻璃仪器有 (填仪器名称)。

②配制0.1 mol/L NaOH溶液时,其正确的操作顺序是(字母表示,每个字母只能用一次) 。
A.将容量瓶盖紧,振荡,摇匀
B.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
C.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
D.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
E.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
F.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
③配制0.1 mol/L NaOH溶液时,在实验中其他操作均正确,若定容时仰视容量瓶刻度线,则所配溶液浓度 0.1 mol/L(填“大于”、“等于”或“小于”)。
④配制0.5 mol/L硫酸溶液500 mL时,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为 mL(计算结果保留一位小数)。
⑤配制0.5 mol/L硫酸溶液时,在实验中其他操作均正确,若用量筒量取浓硫酸时仰视刻度线,则所配溶液浓度 0.5 mol/L(填“大于”、“等于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省五校协作体高一上学期期中化学试卷(解析版) 题型:选择题
下列说法正确的是(NA表示阿伏加德罗常数的值):
①28 g氮气所含有的原子数目为NA
②4 g金属钙变成钙离子时失去的电子数目为0.1 NA
③在常温常压下,11.2 L N2含有的分子数为0.5 NA
④在标准状况下, 1 mol氦气含有的原子数为NA
⑤0.5 mol单质铝与足量盐酸反应转移电子数为1.5NA
⑥标准状况下,1 L水所含分子数为1/22.4NA
⑦17 g氨气所含电子数目为10NA
A.①②⑤⑥⑦ B.①②④⑤⑥ C.⑤⑦ D.④⑤⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com