
 如图的实验装置用来分离CO2和CO气体并干燥.图中a为止水夹,b为分液漏斗的活塞,通过Y型管和止水夹分别接c、d两球胆,现装置内的空气已排尽.为使实验成功,甲、乙、丙分别盛放的溶液是( )
如图的实验装置用来分离CO2和CO气体并干燥.图中a为止水夹,b为分液漏斗的活塞,通过Y型管和止水夹分别接c、d两球胆,现装置内的空气已排尽.为使实验成功,甲、乙、丙分别盛放的溶液是( )| A、NaHCO3饱和溶液 12 mol?L-1盐酸 18.4 mol?L-1H2SO4 | B、Na2CO3饱和溶液 2 mol?L-1H2SO4 NaOH饱和溶液 | C、NaOH饱和溶液 2 mol?L-1H2SO4 18.4 mol?L-1H2SO4 | D、18.4 mol?L-1H2SO4 NaOH饱和溶液 18.4 mol?L-1H2SO4 |


科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
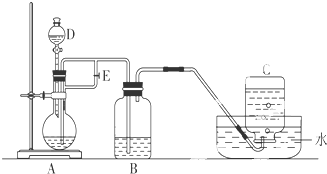
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:

A.NaHCO3饱和溶液;12 mol·L-1盐酸;18.4 mol·L-1 H2SO4
B.Na2CO3饱和溶液;2 mol·L-1 H2SO4;NaOH饱和溶液
C.NaOH饱和溶液;2 mol·L-1 H2SO4;18.4 mol·L-1 H2SO4
D.18.4 mol·L-1 H2SO4;NaOH饱和溶液;18.4 mol·L-1 H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com