
| A. | 2-甲基-4-乙基戊烷 | B. | 3,4,4-三甲基己烷 | ||
| C. | 2,3-二乙基-1-戊烯 | D. | 3,4-二甲基-4-乙基己烷 |
分析 A、烷烃命名时,要选最长的碳链为主链,从离支链近的一端给主链上碳原子编号,据此分析;
B、烷烃命名时,要选最长的碳链为主链,从离支链近的一端给主链上碳原子编号,据此分析;
C、烯烃命名时,要选含官能团的最长的碳链为主链,从离官能团最近的一端给主链上的碳原子编号,并表示出官能团的位置;
D、烷烃命名时,要选最长的碳链为主链,从离支链近的一端给主链上碳原子编号,据此分析.
解答 解:A、烷烃命名时,要选最长的碳链为主链,故此烷烃的主链上有6个碳原子,即为己烷,从离支链近的一端给主链上碳原子编号,故在2号和4号碳原子上各有一个甲基,故名称为:2,4-二甲基己烷,故A错误;
B、烷烃命名时,要选最长的碳链为主链,故主链上有6个碳原子,故为己烷,要从离支链近的一端给主链上碳原子编号,而当两端离支链一样近时,要从支链多的一端给主链上的碳原子编号,故在3号碳原子上有2个甲基,在4号碳原子上有一个甲基,故名称为3,3,4-三甲基己烷,故B错误;
C、烯烃命名时,要选含官能团的最长的碳链为主链,故主链上有5个碳原子,故为戊烯,从离官能团最近的一端给主链上的碳原子编号,故碳碳双键在1号和2号碳原子之间,在2号碳原子和3号碳原子上各有一个乙基,故名称为2,3-二乙基-1-戊烯,故C正确;
D、烷烃命名时,要选最长的碳链为主链,故主链上有6个碳原子,故为己烷,要从离支链近的一端给主链上碳原子编号,而当两端离支链一样近时,要从支链多的一端给主链上的碳原子编号,故在3号碳原子上有1个甲基和1个乙基,在4号碳原子上有一个甲基,故名称为3,4-二甲基-3-乙基己烷,故D错误.
故选C.
点评 本题考查了烷烃和烯烃命名的正误判断,难度不大,应注意的是命名时,烷烃选最长的碳链为主链,而烯烃选含官能团的最长的碳链为主链.


科目:高中化学 来源: 题型:选择题
| A. | 该氯原子的相对原子质量为$\frac{a}{b}$ | |
| B. | m g该氯原子的物质的量为$\frac{m}{a{N}_{A}}$mol | |
| C. | 该氯原子的摩尔质量为aNAg | |
| D. | a g该氯原子所含的电子数为17 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③⑤ | C. | ①和④ | D. | ③和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
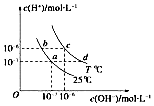
| A. | 若从a点到c点,可采用在水中加入酸的方法 | |
| B. | b点对应的醋酸中由水电离的c(H+)=10-6mol•L-1 | |
| C. | T℃时,0.05 mol•L-1的Ba(OH)2溶液的pH=11 | |
| D. | c点对应溶液的Kw大于d点对应溶液的Kw |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
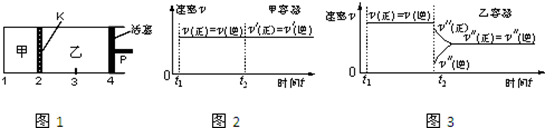
| A. | 保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 | |
| B. | 保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增加 | |
| C. | 保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 | |
| D. | 保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
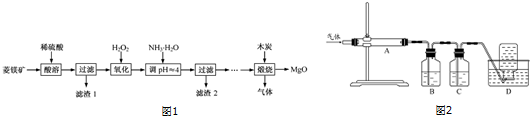
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | COS分子中所有原子都满足8电子稳定结构 | |
| B. | COS与CO2互为等电子体 | |
| C. | COS分子是含有极性键的非极性分子 | |
| D. | COS的结构式为S=C=O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com