
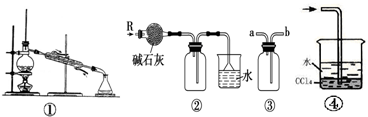
 如图各装置不能达到实验目的是( )
如图各装置不能达到实验目的是( )| A、装置①可制取少量蒸馏水 |
| B、装置②可用于干燥、收集氨气,并吸收多余的氨气 |
| C、装置③可用于排空气法收集NO气体 |
| D、装置④中下层物质若为四氯化碳,则可用于吸收氯化氢 |


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
| A、Na+、CO32-、Ca2+、Cl- |
| B、H+、K+、OH-、NO3- |
| C、H+、Cu2+、OH-、HCO3- |
| D、K+、Na+、Cl-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石墨不如金刚石稳定 |
| B、C(石墨,s)═C(金刚石,s)△H=-3E kJ/mol |
| C、金刚石常温下可转化为石墨 |
| D、等质量的石墨和金刚石完全燃烧,金刚石放出的能量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 |
| B、“雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物无关 |
| C、白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去 |
| D、高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,44 g C3H8中含有的碳碳单键数为3NA |
| B、1mol羟基中电子数为10NA |
| C、室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| D、标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2、NO2和SO2都是酸性氧化物,都是大气污染物 |
| B、常温下,铁在浓硫酸、浓硝酸中均能发生钝化,均能用铁罐储运 |
| C、Na2O2、H2O2所含化学键完全相同,都能作供氧剂 |
| D、NaClO和明矾都能作消毒剂或净水剂,加入酚酞试液均显红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同主族元素从上到下,金属性逐渐增强 |
| B、主族元素的最高正化合价均等于它所在的主族序数 |
| C、同周期的元素(稀有气体例外)的原子半径越小,越难失去电子 |
| D、元素的非金属性越强,其气态氢化物水溶液的酸性越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 能源短缺是人类将要面临的一个重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
能源短缺是人类将要面临的一个重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com