
 .
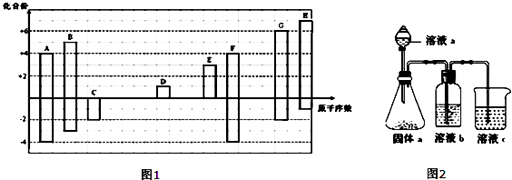
.分析 短周期元素中,A、F均有+4、-4价,处于ⅣA族,且原子序数A<F,故A为碳、F为Si;C、G均有-2价,且G有+6,G的原子序数较大,故C为O元素、G为S元素;B有+5、-3价,原子序数介于碳、氧之间,故B为N元素;H有+7、-1价,原子序数大于硫,则H为Cl;D有+1价,E有+3价,分别处于ⅠA族、ⅢA族,原子序数氧<D<E<Si,故D为Na,E为Al,以此解答该题.
解答 解:短周期元素中,A、F均有+4、-4价,处于ⅣA族,且原子序数A<F,故A为碳、F为Si;C、G均有-2价,且G有+6,G的原子序数较大,故C为O元素、G为S元素;B有+5、-3价,原子序数介于碳、氧之间,故B为N元素;H有+7、-1价,原子序数大于硫,则H为Cl;D有+1价,E有+3价,分别处于ⅠA族、ⅢA族,原子序数氧<D<E<Si,故D为Na,E为Al.
(1)元素F为Si,在周期表中的位置:第三周期ⅣA族,故答案为:第三周期ⅣA族;
(2)O与Na形成原子个数比为1:1的化合物是过氧化钠,过氧化钠中所含有离子键、非极性共价键,过氧化钠为离子化合物,O原子和Na原子之间形成共用电子对,用电子式表示过氧化钠的形成过程为: ,
,
故答案为:离子键、非极性共价键; ;
;
(3)电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越小,简单离子半径大小顺序是:S2->O2->Na+,
故答案为:S2->O2->Na+;
(4)①利用最高价含氧酸的酸性强弱,证明A、B、F的非金属性强弱关系,溶液a为硝酸,溶液b为饱和NaHCO3溶液,溶液c为硅酸钠溶液,
故答案为:硝酸(HNO3);饱和NaHCO3溶液;
②溶液c为硅酸钠溶液,溶液c中的离子反应方程式为:SiO32-+CO2+H2O=H2SiO3↓+CO32-或SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-,
故答案为:SiO32-+CO2+H2O=H2SiO3↓+CO32-或SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-.
点评 本题考查结构性质位置关系应用,为高考常见题型,侧重于学生的分析能力的考查,解答关键是根据化合价与原子序数推断元素,注意对元素周期律的理解掌握,难度中等.


 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温下 pH为5的盐酸溶液稀释 1000倍后,pH 等于8 | |
| B. | 在滴有酚酞溶液的氨水里,加入盐酸至恰好呈无色,则此时溶液的 pH=7 | |
| C. | 浓度均为0.1 mol/L的氨水和氯化铵溶液,水电离出的 c(H+)前者大于后者 | |
| D. | 等浓度的 CH3COOH与 KOH任意比混合:c(K+)+c(H+)=c(OH-)+c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OH | B. | CH3CH2CH2OH | C. | CH3CH(OH)CH3 | D. | (CH3)2CH(CH3)2COH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
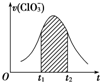 氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.如图为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图.下列说法中不正确的是( )
氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.如图为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图.下列说法中不正确的是( )| A. | 反应开始时速率增大可能是c(H+)所致 | |
| B. | 后期反应速率下降的主要原因是反应物浓度减小 | |
| C. | 纵坐标为v(H+)的v-t曲线与图中曲线完全重合 | |
| D. | 图中阴影部分“面积”可以表示t1-t2时间为c(Cl-)增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
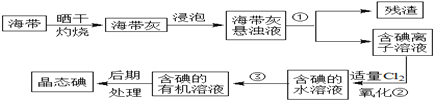
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素非金属性由弱到强的顺序:M、N、Y | |
| B. | 单质Y的熔点高于单质Z的熔点 | |
| C. | 原子最外层电子数由少到多的顺序:Y、Z、X、M、N | |
| D. | 电解N和Z形成的化合物可得到对应的N和Z的单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
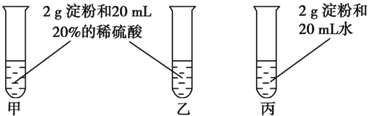
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④⑥⑦ | C. | ②③⑤⑥⑦ | D. | ①③⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的一取代物无同分异构体 | |
| B. | 苯不易跟溴、氯发生加成反应 | |
| C. | 苯分子中碳原子之间以单双键交替存在 | |
| D. | 苯不能使酸性KMnO4溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com