
| 0.82 |
| 0.4×0.4 |
| 0.4mol |
| 0.8mol |
| 0.8mol |
| 0.4mol+0.4mol+0.8mol |
| 0.75mol |
| 1L |


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案科目:高中化学 来源: 题型:
| A、同压强、同温度的O2和O3 |
| B、同温度、同体积的NH3和N2 |
| C、同体积、同密度的C2H4和C3H6 |
| D、同压强、同体积的N2O和CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
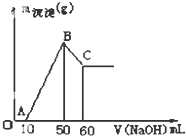 把一小块镁铝金溶于100mL盐酸中,然后向其中滴入1mol?L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.
把一小块镁铝金溶于100mL盐酸中,然后向其中滴入1mol?L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(△H2-△H3):(△H1-△H3) |
| B、(△H3-△H2):(△H1-△H3) |
| C、(△H3-△H2):(△H3-△H1) |
| D、(△H1-△H2):(△H3-△H2) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com