
| A. | 如图,丙烷、丙烯、丙炔的结构分别表示为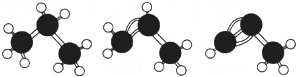 | |
| B. | 相同物质的量的三种物质完全燃烧,生成的气体在标准状态下,体积比3:2:1 | |
| C. | 丙烷、丙烯、丙炔三种物质的熔沸点逐渐升高,相同条件下密度逐渐增大 | |
| D. | 丙炔的碳原予空间结构呈线性排列 |
分析 A.丙炔的球棍模型错误,三个碳原子在一条直线上;
B.相同物质的量的3种物质完全燃烧,标准状况下生成的气体为CO2,三者碳原子相同,所以生成CO2体积相同;
C.相对分子质量越大,熔沸点越高;
D.丙炔中的碳原子是sp杂化,为直线形.
解答 解:A.丙炔的球棍模型中,三个碳原子应该在同一条直线上,故A错误;
B.相同物质的量的3种物质完全燃烧,标准状况下生成的气体为CO2;三者碳原子相同,所以生成CO2体积相同,体积比为1:1:1,故B错误;
C.丙烷、丙烯、丙炔三种物质的相对分子量逐渐减小,其熔沸点逐渐降低,故C错误;
D.丙炔中的碳原子是sp杂化,丙炔的碳原子空间结构是直线形的,故D正确;故选D.
点评 本题考查了丙烷、丙烯、丙炔的结构和性质,题目难度不大,注意根据丙烷、丙烯和丙炔的组成及结构差别进行分析即可.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
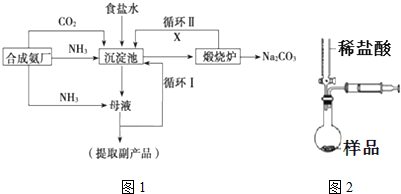
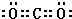 ,沉淀池中发生的化学反应方程式为:CO2+NH3+NaCl+H2O═NaHCO3↓+NH4Cl.
,沉淀池中发生的化学反应方程式为:CO2+NH3+NaCl+H2O═NaHCO3↓+NH4Cl.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用可降解塑料制品 | |
| B. | 工业废气排入大气 | |
| C. | 对化石燃料进行综合利用 | |
| D. | 尽量采取步行、骑自行车或乘坐公共交通工具等方式出行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤、石油和天然气都是重要的化石燃料 | |
| B. | 蚕丝、塑料和橡胶均属于合成高分子材料 | |
| C. | 淀粉、麦芽糖和蛋白质均能发生水解反应 | |
| D. | 糖类、油脂和蛋白质都含有C、H、O三种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5:3 | B. | 5:4 | C. | 1:1 | D. | 3:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂是热值最高的营养物质 | |
| B. | 苯和乙醇都能发生氧化反应 | |
| C. | 聚乙烯能使酸性高锰酸钾溶液褪色 | |
| D. | 用Na2CO3溶液可以区分CH3COOH和CH3COOCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | ① | ② | ③ | 实验结论 | 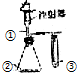 |
| A | 稀盐酸 | Na2SO4 | 溴水 | SO2具有漂白性 | |
| B | 浓氨水 | CaO | AlCl3溶液 | 白色沉淀生成后又溶解 | |
| C | 双氧水 | MnO2 | KI溶液 | 氧化性:O2>I2 | |
| D | 稀醋酸 | Na2CO3 | Na2SiO3溶液 | 酸性:醋酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com