
下列说法或计算正确的是 ( )
A、采用加热蒸发溶剂的方法可以使浓度为2mol/L的氢溴酸溶液的浓度变为4mol/L
B、m g H2和n g He,在同温同压下密度之比等于m:n
C、只有标准状况下,等物质的量的乙烯和一氧化碳所含的分子数才相等
D、将a%的某物质的水溶液加热蒸发掉m g水(溶质不挥发,且蒸发过程中无溶质析出),所得溶液体积为V L,溶质的质量分数为蒸发前的2倍.设溶质的相对分子质量为M,则蒸发后所得溶液的物质的量浓度为![]()
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源:安徽省省城名校2012届高三第三次联考试题化学试题 题型:058
Ⅰ.如图所示,50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L,NaOH溶液在装置中进行中和反应.通过测定反应过程中所放出的热量,可计算中和热,回答下列问题:
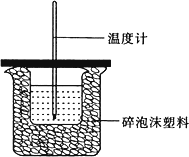
(1)图中装置缺少的仪器是________.
(2)下列说法中不正确的是________.(填字母,下同)
A.若用50 mL 0.55 mol·L-1的Ba(OH)2溶液代替NaOH溶液进行实验,测得的中和热是相同的
B.若用50 mL 0.50 mol·L-1的醋酸溶液代替盐酸进行实验,测得的中和热是相同的
C.若分别用等浓度的硫酸和Ba(OH)2溶液代替盐酸和NaOH溶液进行实验,测得的中和热是相同的
D.NaOH溶液稍过量的原因是让盐酸完全反应
Ⅱ.某学生用0.1 mol·L-1的盐酸标准溶液滴定未知浓度的20.00 mL氨水,用酚酞做指示剂,回答下列问题:
(1)在滴定时,左手握________(填仪器名称)的活塞,右手摇动锥形瓶,眼睛注视________.直到最后加入一滴盐酸后,溶液出现________现象,说明达到滴定终点,记录数据,发现消耗盐酸25.00 mL.
(2)下列操作中可能使所测氨水溶液的浓度数值偏低的是________.
A.酸式滴定管未用标准盐酸润洗,就直接注入标准盐酸
B.滴定前盛放氨水的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)当盐酸与氨水恰好完全反应生成盐时,消耗的盐酸溶液体积V________(填“>”、“<”或“=”)25.00 mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业的核心反应是:
能量变化如右图,回答下列问题:
(1)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1 ,E2 (填“增大”、“减小”、“不变”)
(2)在500℃、2×107Pa和催化剂条件下向一密闭容器中充入0.5mol N2和1.5mol H2,充分反应后,放出的热量 (填“<”、“>”或“=”)46.2kJ;
(3)关于该反应的下列说法中,正确的是 。
A.△H>0,△S>0 B.△H>0,△S< 0 C.△H<0,△S>0 D.△H<0,△S<0(4)将一定量的N2(g)和H2(g)放入 1L密闭容器中,在500℃、2×107Pa下达到平衡,测得N2为0.10mol,H2为0.30mol,NH3为0.10mol。计算该条件下达到平衡时H2转化为NH3的转化率 。若升高温度,K值变化 (填“增大”、“减小”或“不变”)。
(5)在上述(4)反应条件的密闭容器中,欲提高合成氨中H2的转化率,下列措施可行的是 (填字母)。
A.向容器中按原比例再充入原料气 B.向容器中再充入惰性气体
C.改变反应的催化剂 D.分离出氨
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮专题冲刺第6讲 化学反应速率和化学平衡练习卷(解析版) 题型:填空题
合成氨工业的核心反应是:N2(g)+3H2(g)  2NH3(g) ΔH=Q kJ·mol-1,能量变化如下图,回答下列问题:
2NH3(g) ΔH=Q kJ·mol-1,能量变化如下图,回答下列问题:

(1)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1________,E2________(填“增大”、“减小”或“不变”)。
(2)在500℃、2×107Pa和催化剂条件下向一密闭容器中充入0.5 mol N2和1.5 mol H2,充分反应后,放出的热量________ 46.2 kJ(填“<”、“>”或“=”)。
(3)关于该反应的下列说法中,正确的是________。
A.ΔH>0,ΔS>0??????? B.ΔH>0,ΔS<0
C.ΔH<0,ΔS>0????? ? D.ΔH<0,ΔS<0
(4)将一定量的N2(g)和H2(g)放入1 L密闭容器中,在500℃、2×107Pa下达到平衡,测得N2为0.10 mol,H2为0.30 mol,NH3为0.10 mol。计算该条件下达到平衡时H2转化为NH3的转化率________。若升高温度,K值变化________(填“增大”、“减小”或“不变”)。
(5)在上述(4)反应条件的密闭容器中,欲提高合成氨中H2的转化率,下列措施可行的是________(填字母)。
A.向容器中按原比例再充入原料气
B.向容器中再充入惰性气体
C.改变反应的催化剂
D.分离出氨气
查看答案和解析>>
科目:高中化学 来源:2011-2012学年沈阳铁路实验中学高三上学期第三次月考化学试卷 题型:填空题
合成氨工业的核心反应是:
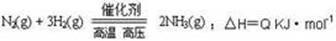
能量变化如右图,回答下列问题:
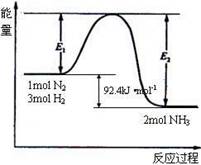
(1)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1 ,E2 (填“增大”、“减小”、“不变”)
(2)在500℃、2×107Pa和催化剂条件下向一密闭容器中充入0.5mol N2和1.5mol H2,充分反应后,放出的热量 (填“<”、“>”或“=”)46.2kJ;
(3)关于该反应的下列说法中,正确的是 。
A.△H>0,△S>0 B.△H>0,△S< 0 C.△H<0,△S>0 D.△H<0,△S<0(4)将一定量的N2(g)和H2(g)放入 1L密闭容器中,在500℃、2×107Pa下达到平衡,测得N2为0.10mol,H2为0.30mol,NH3为0.10mol。计算该条件下达到平衡时H2转化为NH3的转化率 。若升高温度,K值变化 (填“增大”、“减小”或“不变”)。
(5)在上述(4)反应条件的密闭容器中,欲提高合成氨中H2的转化率,下列措施可行的是 (填字母)。
A.向容器中按原比例再充入原料气 B.向容器中再充入惰性气体
C.改变反应的催化剂 D.分离出氨
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com