
| A、PMNE | B、ENMP |
| C、PNME | D、EPMN |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是一个电解装置图,某实验兴趣小组做完实验后,在读书卡片上写下了一些记录:( )
如图是一个电解装置图,某实验兴趣小组做完实验后,在读书卡片上写下了一些记录:( )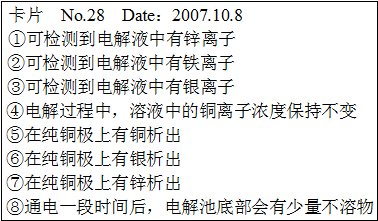 卡片上描述合理的是(已知粗铜中除含有铜以外,还含有少量锌、铁、银)
卡片上描述合理的是(已知粗铜中除含有铜以外,还含有少量锌、铁、银)| A、①②⑤⑧ | B、①⑤⑧ |
| C、①②④⑤⑧ | D、③⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、△H1=△H2=△H3 | ||
B、△H1<△H2,△H3=
| ||
| C、△H1>△H2,△H2=2△H3 | ||
| D、无法比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O3+2KI+H2O═2KOH+I2+O2 |
| B、2CH3COOH(醋酸)+Ca(ClO)2═2HClO+(CH3COO)2Ca |
| C、I2+2NaClO3═2NaIO3+Cl2 |
| D、4HCl(浓)+MnO2=△=MnCl2+Cl2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3Cl2+6KOH═5KCl+KClO3+3H2O |
| B、2NO2十2NaOH═NaNO3+NaNO2+H2O |
| C、SnCl4+2H2O═SnO2+4HCl |
| D、3CCl4+K2Cr2O7═2CrO2Cl2+3COCl2+2KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、28gN2所含有的原子数为1NA |
| B、常温常压下,1molCO2气体中所含有的分子数不等于1NA |
| C、46gNO2和N2O4的混合物中含有的分子数为1NA |
| D、0.1molNH4+所含有的电子数为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l);△H=-1135.7kJ/mol | ||
| B、2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=-1000.3kJ/mol | ||
C、N2H4(g)+NO2(g)=
| ||
| D、2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=-1135.7kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com