
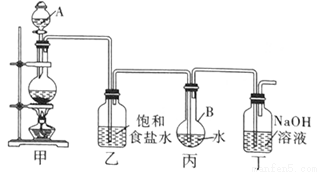
(1)写出装置甲中发生反应的化学方程式: 。
装置甲中的仪器使用前需要检漏的有 (写名称)。
(2)利用装置丙制取饱和氯水并测其pH值。
①证明氯水已饱和的现象是 。
②测定饱和氯水的pH方法是 。
③若撤去装置乙,直接将装置甲和丙相连。这样做对实验测定结果的影响是 。
(3)饱和氯水与石灰石的反应是制取较浓的HClO溶液的方法之一。某同学运用这一方法,尝试制取HClO溶液并进行了如下定性实验:
i.在试管中加入过量的块状碳酸钙,再加入约20ml饱和氯水,充分反应,有少量气泡产生,溶液的黄绿色褪去;
ii.过滤,将滤液滴在有色布条上,发现其漂白性更强;
iii.为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立刻产生大量气泡;
第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2气体。
② 试解释可以在饱和氯水中加入石灰石制备HClO的原因: 。(用有关的方程式结合文字回答)
②试根据所学知识推测,在ii的滤液中含有的溶质,除了溶解的极少量氯气外,还含有的其他溶质为 (写化学式)。
③写出步骤iii中第一份滤液发生反应的离子方程式: 。
 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源:2015-2016学年吉林省高二下学期基础训练(15)化学试卷(解析版) 题型:填空题
(1)质量相同的O2、NH3、H2、Cl2四种气体中,在相同温度和相同压强条件下,体积最大的是 。
(2)下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是 。(填序号)
①NaAlO2②Ca(OH)2③Na2CO3④Al(OH)3⑤NaHCO3⑥Si
(3)氯水中含有多种成分。将紫色石蕊试液滴入氯水中,溶液显红色起作用的成分是 ;过一会儿,溶液颜色逐渐褪去,起作用的成分是 ;
(4)已知:Fe2+的还原性强于Br—,标准状况下把11.2L氯气通入500ml 0.8mol/L FeBr2溶液中,写出反应完全后的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期基础训练(15)化学试卷(解析版) 题型:选择题
将氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,通过一步实验就能加以区别,并只用一种试剂,这种试剂是
A. KSCN B. BaCl2 C. NaOH D. HCl
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省西安市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列离子方程式或电离方程式的书写正确的是( )
A. NaHSO4熔融:NaHSO4 = Na++H++SO42-
B. Al(OH)3酸式电离:Al(OH)3 = 3OH—+Al3+
C. 向Na2CO3溶液中滴入少量稀盐酸:CO32-+2H+ = H2O+CO2↑
D. Ca(HCO3)2溶液与少量NaOH溶液反应:OH-+HCO +Ca2+ = CaCO3↓+H2O
+Ca2+ = CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省西安市高一上学期期末考试化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A. 28g N2所含有的原子数为NA
B. 标准状况下,22.4 L水中含有的水分子数为NA
C. 500 mL 1.0 mol/L碳酸钠溶液中所含Na+的数为0.5NA
D. 49g纯硫酸所含有的氧原子数与标况下22.4L CO2中所含有的氧原子数相等
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省衡阳市高二理科实验班下学期第一次月考理综化学试卷(解析版) 题型:选择题
将反应5IO3-+I-+6H+ 3I2+3H2O设计成如下图所示的原电池。开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流计指针再次发生偏转。
3I2+3H2O设计成如下图所示的原电池。开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流计指针再次发生偏转。
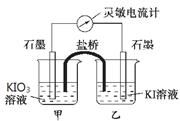
下列判断不正确的是
A. 开始加入少量浓硫酸时,乙中石墨电极上发生氧化反应
B. 开始加入少量浓硫酸时,同时在甲、乙烧杯中都加入淀粉溶液,只有乙烧杯中溶液变蓝。
C. 电流计读数为零时,反应达到化学平衡状态
D. 两次电流计指针偏转方向相反
查看答案和解析>>
科目:高中化学 来源:2017届河南省天一大联考高三阶段性测试(四)(b卷)理综化学试卷(解析版) 题型:简答题
碳及其化合物在人们的日常生活、工农业生产及科学研究中有着重要的作用。回答下列有关问题:
(1)煤炭是人们利用最为广泛的燃料,但因煤炭含硫而导致大气污染。对燃煤烟气中的SO2可采用碳酸钙浆液法吸收,即把燃煤烟气和空气同时鼓入到含CaCO3的浆液中,使SO2被吸收。①该反应生成石膏(CaSO4 •2H2O),化学方程式为____________________。
②标准状况下,某种烟气中SO2含量为2.1×10-3g •L-1,则反应中转移3 mol电子时,处理标
准状况下烟气的体积为___________L(保留两位有效数字)。
(2)工业炼铁的基本原理是:在高温下,焦炭燃烧生成的CO将铁矿石中铁的氧化物还原得到铁。
已知:
①Fe2O3(s)+3C(s,石墨)==2Fe(s)+3CO(g) △H= +489.0 kJ• mol-1;
②C(s,石墨)+CO2(g) ==2CO(g) △H= +172.5 kJ• mol-1。
则CO还原Fe2O3(s)的热化学方程式为_______________________。
(3)碳酸二甲酯(DMC)是一种无毒、环保性能优异、用途广泛的化工原料。一定温度时,在容积为1.0 L的恒容密闭容器中充入2.5molCH3OH(g)、适量CO2和5×10-3催化剂,容器中发生反应:2CH3OH(g) +CO2(g)  CH3OCOOCH3(g) +H2O(g) △H= -15.5kJ• mol-1。甲醇转化数(TON)与反应时间的关系如图1所示:
CH3OCOOCH3(g) +H2O(g) △H= -15.5kJ• mol-1。甲醇转化数(TON)与反应时间的关系如图1所示:
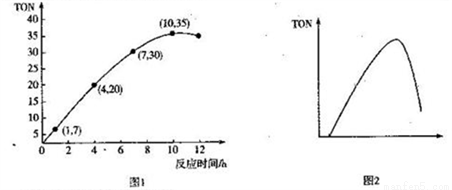
已知:TON=
①该温度时,甲醇的最高转化率为_______________。
② 0 ~7 h内DMC的平均反应速率是_______mol·L-1·h-1(保留两位有效数字)。
③图2是甲醇转化数随某种物理量的变化曲线,该物理量可能是_______;为使该反应向正
反应方向移动,可采取的措施有______________________。(答出一条即可)。
(4)CO2溶解于水形成碳酸。碳酸与次氯酸的电离常数如下表所示:
弱酸 | 碳酸 | 次氯酸 |
电离常数(Ka) | Ka1=4.4×l0-7 Ka2=5.6×10-11 | 3.0×10-8 |
在NaClO溶液中通入少量CO2 ,反应的离子方程式为_____________________,0.03 mol • L-1 NaClO 溶液的 pH=________________。
查看答案和解析>>
科目:高中化学 来源:浙江省衢州市2017届高三1月教学质量检测化学试卷 题型:选择题
向含amolNaOH和amolNa2CO3的混合溶液中通入bmolCO2充分反应(不考虑CO2的溶解),下列说法不正确的是
A. 当a≥2b时,发生的离子反应为:2OH-+CO2=CO32-+H2O
B. 当a=1.25b时,发生的离子方程式为:5OH-+4CO2=3HCO3-+CO32-+H2O
C. 2b/3<a<2b时,溶液中CO32-与HCO3-物质的量之比为:(2b-a):(2a-b)
D. 若反应后溶液中CO32-与OH-物质的量之比为2:1,则5b=a
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省南京市高二学业水平模拟测试化学试卷(解析版) 题型:选择题
下列关于乙醇性质的说法正确的是
A. 乙醇是无色无味的液体 B. 乙醇能使紫色石蕊试液变红
C. 乙醇不能与金属钠反应 D. 乙醇能被酸性高锰酸钾溶液氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com