
水是生命之源,也是化学反应中的主角。请回答下列问题:
Ⅰ、氢气燃烧生成液态水热化学方程式是2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ/mol。
(1)生成物能量总和(填“大于”、“小于”或“等于”)反应物能量总和。
(2)若2 mol氢气完全燃烧生成水蒸气,则放出的热量 572 kJ(填“>”、“<”或“=”)。
(3)氢气热值为 。
Ⅱ、氢气和氧气反应生成水,将化学能转化为电能,其构造如图所示:a、b两个电极均由多孔的碳块组成。

(1)a电极反应式是
(2)b电极反应式是
Ⅲ、如图表示一个电解池。X、Y都是惰性电极,电解液a是饱和食盐水,同时在两边各滴入几滴酚酞试液。

(1)X极上的电极反应式为 ,
在X极附近观察到的现象是 。
(2)Y极上的电极反应式为 ,
检验该电极反应产物的方法是 。
Ⅰ(1) 小于(2) <(3) 143 kJ/g
Ⅱ、(1) H2-2e- + 2OH-=2H2O(2)O2 + 4e- + 2H2O=4OH-
Ⅲ、(1) 2H+ + 2e-=H2↑ 或2H2O + 2e-=H2+2OH-↑;产生气泡,溶液变红
(2) 2Cl-- 2e-=Cl2↑;用湿润的淀粉碘化钾试纸检验,试纸变蓝(其它合理方法亦可)
【解析】
试题分析:Ⅰ、(1)该反应正反应为放热反应,生成物的总能量小于反应物总能量。(2)气态水的能量高于液体水,故生成2mol气态水放出的热量小于572kJ。(3)值指1kg燃料完全燃烧放出的热量,由热化学方程式可知,1kg氢气燃烧放出的热量为 ,故氢气的热值为143kJ/g。
,故氢气的热值为143kJ/g。
Ⅱ、(1)a极通入H2,发生氧化反应,在碱性条件下生成水,电极反应式为:H2 + 2OH– – 2e–=2H2O。(2)b极通入O2,发生还原反应,生成OH–,电极反应式为:O2 + 2H2O + 4e–=4OH–。
Ⅲ、(1)X极连接电源的负极,为阴极,发生还原反应,H2O电离产生的H+在X极放电生成H2,同时生成OH–,电极反应式为:2H2O + 2e–=H2↑ + 2OH–,溶液呈碱性,故可观察到的现象为:产生气泡,溶液变红色。(2)Y极连接电源的正极,为阳极,发生氧化反应,Cl–在Y极放电生成Cl2,电极反应式为:2Cl--2e-=Cl2↑,用湿润的淀粉KI试纸检验,试纸变蓝。
考点:本题考查热化学方程式、原电池、电解池等知识。


科目:高中化学 来源: 题型:阅读理解
| 键型 | 键能 (kJ/mol) |
键长 (pm) |
分子 | 键角 | 物质 | 熔点(℃) | 沸点(℃) |
| H-C | 413 | 109 | 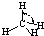 |
109.5° | 甲烷 | -183.7 | -128.0 |
| H-N | 391 | 101 | 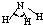 |
107° | 氨 | -77.7 | -33.3 |
| H-O | 467 | 96 |  |
104.5° | 水 | 0.0 | 100.0 |
查看答案和解析>>
科目:高中化学 来源:黑龙江省哈尔滨三中2010届高三9月月考化学试题 题型:022
水是生命之源,也是一种常用的试剂.请回答下列问题:
(1)水分子中氧原子在基态时核外电子排布式为________.
(2)H2O分子中氧原子采取的是________杂化.
(3)水分子容易得到一个H+形成水合氢离子(H3O+).对上述过程的下列描述不合理的是________.
A.氧原子的杂化类型发生了改变
B.微粒的空间构型发生了改变
C.微粒中的键角发生了改变
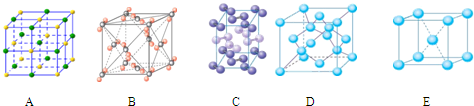
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序).与冰的晶体类型相同的是________.(请用相应的编号填写)

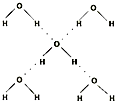
(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是________kJ/mol.
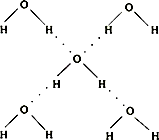
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子.请写出生成此配合离子的离子方程式:________.
查看答案和解析>>
科目:高中化学 来源:2012-2013年辽宁实验中学分校高二下学期阶段性测试化学试卷(带解析) 题型:填空题
水是生命之源,也是一种常用的试剂。请回答下列问题:
(1)水分子中氧原子在基态时核外电子排布式为___ _______;
(2)H2O分子中氧原子采取的是 杂化。
(3)水分子容易得到一个H+形成水合氢离子(H3O+)。对上述过程的下列描述不合理的是 。
| A.氧原子的杂化类型发生了改变 | B.微粒的形状发生了改变 |
| C.水合氢离子分子构型是三角锥型 | D.微粒中的键角发生了改变 |
查看答案和解析>>
科目:高中化学 来源:2014届辽宁实验中学分校高二下学期阶段性测试化学试卷(解析版) 题型:填空题
水是生命之源,也是一种常用的试剂。请回答下列问题:
(1)水分子中氧原子在基态时核外电子排布式为___ _______;
(2)H2O分子中氧原子采取的是 杂化。
(3)水分子容易得到一个H+形成水合氢离子(H3O+)。对上述过程的下列描述不合理的是 。
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.水合氢离子分子构型是三角锥型 D.微粒中的键角发生了改变
(4)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
水是生命之源,也是一种常用的试剂。请回答下列问题:
(1)水分子中氧原子在基态时核外电子排布式为 。
(2)H2O分子中氧原子采取的是 杂化。
(3)水分子容易得到一个H+形成水合氢离子(H3O+)。对上述过程的下列描述不合理的是 。
A.氧原子的杂化类型发生了改变 B.微粒的空间构型发生了改变
C.微粒中的键角发生了改变
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是______。(请用相应的编号填写)
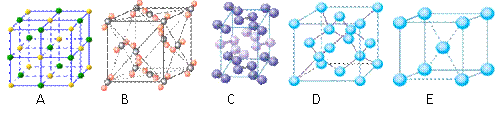 |

(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是_________kJ/mol。
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com