
向FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是
A.加入KSCN溶液一定不变红色 B.溶液中一定含Fe2+
C.溶液中一定含Cu2+ D.剩余固体中一定含Cu
科目:高中化学 来源:2016届江西省红色七校高三上学期第一次联考化学试卷(解析版) 题型:选择题
下列实验操作与预期实验目的或所得实验结论一致的是
实验操作 | 实验目的或结论 | |
A | 某钾盐某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 说明该钾盐是K2CO3 |
B | 向含有含少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一段时 间后过间后过滤 | 除去MgCl2溶液中少量 FeCl3 |
C | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中 加稀盐酸,有气泡产生 | 说明常温下 Ksp(BaCO3)< Ksp(BaSO4) |
D | C2H5OH乙醇与浓硫酸170 ℃共热,制得的气体通入酸性KMnO4溶液 | 检验制得气体是否为乙烯 |
查看答案和解析>>
科目:高中化学 来源:2016届江苏省淮安市高三上学期9月月考化学试卷(解析版) 题型:选择题
某反应的反应过程中能量变化如右图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是
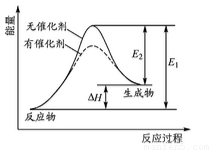
A.该反应为放热反应
B.催化剂能改变反应的焓变
C.逆反应的活化能大于正反应的活化能
D.催化剂能降低反应的活化能
查看答案和解析>>
科目:高中化学 来源:2016届湖南省常德市高三上学期10月月考化学试卷(解析版) 题型:选择题
某固体物质A在一定条件下受热分解产物都是气体,有关的化学方程式为:2A=B↑+2C↑+2D↑。若生成的混合气体对氘气的相对密度为d,则A的相对分子质量为
A.2d B.2.5d C.5d D.10d
查看答案和解析>>
科目:高中化学 来源:2016届湖南省浏阳市高三上学期第二次月考化学试卷(解析版) 题型:填空题
(10分)W、M、X、Y、Z五种短周期元素在周期表中的位置如图所示:
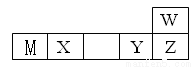
其中只有M为金属元素,请回答下列问题:
(1)M在元素周期表中的位置为 ,比较Y与Z两种元素的简单离子的半径大小 (用离子符号表示)。
(2)写出X的氧化物与W的氢化物的水溶液反应的化学方程式 。
(3)科学家研制出一种新型分子C16Y8(结构如图所示)
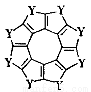
它将成为潜在的储氢材料。1molC16Y8最多能与 molH2发生加成反应。
(4)一种名贵黄石组成为M2(XO4)WOH,在强碱性溶液中会发生腐蚀,写出其过量NaOH溶液反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上学期二次模拟测试理综化学试卷(解析版) 题型:填空题
元素周期表的用途广泛。
(1)用“>”或“<”填空:
离子半径 | 非金属性 | 熔点 | 沸点 |
K+_____S2- | N____O | 金刚石_____晶体硅 | HF____HCl |
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是 (填序号)。
a.Cl2、Br2、I2的熔点 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液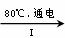 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体
①完成I中反应的总化学方程式:□NaCl+□H2O=□NaClO3+□ 。
②II中转化的基本反应类型是 ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
(4)一定条件,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(KJ)相对大小如右图所示。
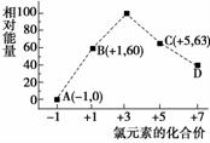
①D是 (填离子符号)。
②B→A+C反应的热化学方程式为 (用离子符号表示)
查看答案和解析>>
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第三次月考化学试卷(解析版) 题型:选择题
下表中“实验操作”与“预期现象”对应关系正确的是
选项 | 试剂和操作 | 现象 |
A | 向AlCl3溶液中滴入过量的氨水 | 溶液先有白色沉淀,后来沉淀消失 |
B | 向新生成的AgC1浊液中滴入KI溶液,振荡 | 白色沉淀逐渐转化为黄色沉淀 |
C | 向Ca(C1O)2溶液中先通入CO2,再加入少量品红溶液 | 溶液先变浑浊,通入CO2后品红的红色不褪去 |
D | 向BaC12溶液中先通入SO2,再通入过量NO2 | 先生成沉淀,后来沉淀消失 |
查看答案和解析>>
科目:高中化学 来源:2016届安徽省安庆市高三上学期第一次质检化学试卷(解析版) 题型:填空题
(11分)四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数这比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是_________、_________;杂化轨道分别是__________、_________;a分子的立体结构是___________。
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是________晶体,_________晶体。
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)__________。
(4)Y与Z比较,电负性较大的_________,
(5)W元素的化学式__________,其+2价离子的核外电子排布式是___________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上学期10月月考化学试卷(解析版) 题型:选择题
常温下,有下列四种溶液:①pH=2的HCl溶液;②pH=2的CH3COOH溶液;③pH=12的NaOH溶液;④pH=12的氨水。下列有关说法不正确的是
A.将等体积的四种溶液分别稀释100倍,所得溶液的pH:③>④>②>①
B.取体积相同的溶液①、②、③分别与足量铝粉反应,生成H2的量:①最少
C.四种溶液中的KW相同,由水电离出的c(H+):①=②=③=④
D.将VaL溶液①与VbL溶液③混合后,若混合后溶液pH=3,则Va∶Vb=11∶9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com