
| A. | 从C(石墨)=C(金刚石)△H=1.9 kJ•mol-1,可知金刚石比石墨更稳定 | |
| B. | 已知2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol,则H2的燃烧热为285.8 kJ/mol | |
| C. | 在稀溶液中:H++OH-═H2O△H=-57.3kJ•mol-1,若将含1mol CH3COOH的醋酸溶液与含1 mol Ba(OH)2的溶液混合,放出的热量小于57.3 kJ | |
| D. | 图中a曲线表示合成氨(放热反应)使用催化剂时,反应过程中的能量变化 |
分析 A.物质能量越高,稳定性越差,该反应为吸热反应,石墨能量小于金刚石;
B.根据热化学方程式的意义和书写方法来判断,燃烧热是25摄氏度,101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量;
C.乙酸是弱酸,电离过程是吸热过程;
D.催化剂改变反应历程,降低反应的活化能,加快反应速率,该反应是放热反应,应反应物的总能量大于生成物的总能量.
解答 解:A.从C(石墨)═C(金刚石)△H=+1.9kJ/mol,可知石墨具有的能量较低,物质具有的能量越低越稳定,所以石墨比金刚石更稳定,故A错误;
B.2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol,即2molH2完全燃烧生成液态水放出571.6kJ热量,则1molH2燃烧放出的热量285.8kJ,H2的燃烧热为285.8 kJ/mol,故B正确;
C.乙酸是弱酸,电离过程是吸热过程,含1mol CH3COOH的溶液与含1mol NaOH的稀溶液混合,放出热量小于57.3 kJ,故C正确;
D.催化剂改变反应历程,降低反应的活化能,图象a活化能减小,a使用了催化剂,该反应是放热反应,应反应物的总能量大于生成物的总能量,但图象描述是吸热反应,故D错误;
故选AD.
点评 本题考查了物质稳定性与能量高低的关系、燃烧热、中和热等,注意中和热的测定实验中使用的是强酸和强碱的稀溶液,题目难度中等,侧重于考查学生对基础知识的应用能力.


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:解答题

 与足量NaOH溶液反应的化学方程式为CH3CBr(COOH)CH3+2NaOH→CH3C(OH)(COONa)CH3+NaBr+H2O.
与足量NaOH溶液反应的化学方程式为CH3CBr(COOH)CH3+2NaOH→CH3C(OH)(COONa)CH3+NaBr+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④ | C. | ①②③④ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
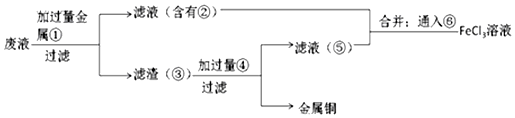
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 氢氧化钠和盐酸的反应 | |
| B. | Ba(OH)2•8H2O晶体和NH4Cl晶体的反应 | |
| C. | 铝与NaOH溶液的反应 | |
| D. | 甲烷在氧气中燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ③④⑥ | C. | ①②③ | D. | ①②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴在铜片上:Cu+2H+=Cu2++H2 | |
| B. | 向20mL0.5mol•L-1FeBr2溶液中通入224mL Cl2(标准状况):2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| C. | Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| D. | NH4Al(SO4)2溶液中加入Ba(OH)2溶液至恰好使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | C | D |
| ①能使溴的四氯化碳溶液褪色 ②比例模型为:  ③能与水在一定条件下反应生成C | ①由C、H两种元素组成; ②球棍模型为:  | ①由C、H、O两种元素组成; ②能与Na反应,但不能与NaOH溶液反应 ③能与D反应生成相对分子质量为100的酯 | ①由C、H、O两种元素组成; ②球棍模型为:  |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com