
在密闭容器中盛有HI气体,在400℃时建立如下平衡:2HI(g)⇌H2 (g)+I2 (g);△H>0,改变下列条件,请填空:(填写变化情况)
(1)将温度升至480℃,混合气体的颜色 ,(加深,变浅、不变)HI的分解率 ,(增大、减小、不变),化学平衡向 移动,平衡常数 (增大、减小、不变),混合气体的总质量 (增大、减小、不变);
(2)若将密闭容器的体积压缩了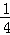 ,平衡常数 (增大、减小、不变)
,平衡常数 (增大、减小、不变)
考点:
化学平衡的影响因素.
专题:
化学平衡专题.
分析:
(1)化学平衡是气体体积不变的吸热反应,升高温度平衡向正向进行,依据平衡移动方向分析碘化氢分解率,混合气体质量守恒,平衡常数随温度变化;
(2)平衡常数随温度变化,不随浓度变化.
解答:
解:(1)在400℃时建立如下平衡:2HI(g)⇌H2 (g)+I2 (g);△H>0,反应是气体体积不变的吸热反应,将温度升至480℃,平衡向吸热反应进行,平衡正向进行,碘单质浓度增大,颜色变深,碘化氢分解率增大,平衡常数不变,反应前后都是气体,混合气体质量不变,
故答案为:变深;增大;向正反应方向;增大;不变;
(2)若将密闭容器的体积压缩了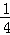 ,压强增大,平衡常数不变,故答案为:不变.
,压强增大,平衡常数不变,故答案为:不变.
点评:
本题考查了化学平衡影响因素的分析判断,主要是平衡常数的分析应用,注意平衡常数随温度变化,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:
如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )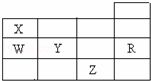
A. 常压下五种元素的单质中,Z单质的沸点最高
B. Y、Z的阴离子电子层结构都与R原子的相同
C. W的氢化物的稳定性比X的氢化物的稳定性高
D. Y元素的非金属性比W元素的非金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属的说法中,正确的是( )
①纯铁较生铁不易生锈;
②冶炼铝和钠都可以用电解法;
③KSCN溶液可以检验Fe3+离子;
④缺钙会引起骨质疏松,缺铁会引起贫血;
⑤青铜、不锈钢、硬铝都是合金;
⑥铜与硫反应,生成黑色的CuS.
A. ①②③④⑤ B. ②③④⑤⑥ C. ①③④⑤ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
反应:X(气)+3Y(气)⇌2Z(气)+热量,在不同温度、不同压强(P1>P2)下,达到平衡时,混和气体中Z的百分含量随温度变化的曲线应为( )
|
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
反应:A(气)+3B(气)⇌2C(气)△H<0达平衡后,将气体混合物的温度降低.下列叙述中正确的是( )
|
| A. | 正反应速率加大,逆反应速率变小,平衡向正反应方向移动 |
|
| B. | 正反应速率变小,逆反应速率加大,平衡向逆反应方向移动 |
|
| C. | 正反应速率和逆反应速率变小,平衡向正反应方向移动 |
|
| D. | 正反应速率和逆反应速率变小,平衡向逆反虑方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有一种气体的质量是14.2g,体积是4.48升(标准状况),该气体的摩尔质量是 ( )
A.28.4 g B.28.4g·mol-1 C.71 g·mol-1 D.71 g
查看答案和解析>>
科目:高中化学 来源: 题型:
同温同压下两个容积相等的贮气瓶,一个装有CO,一个装有N2和C2H4的混合气体,两瓶气体一定不相同的是: ( )
A.分子总数 B.总质量 C.原子总数  D.密度
D.密度
查看答案和解析>>
科目:高中化学 来源: 题型:
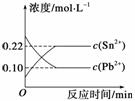 25 ℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
25 ℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
A.往平衡体系中加入金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0
D.25 ℃时,该反应的平衡常数K=2.2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,错误的是( )
A. 任何化学反应都伴随物质变化和能量变化
B. 反应物的总能量低于生成物的总能量时,发生的是吸热反应
C. 有些放热反应也需要加热才能发生
D. 原电池在工作时,电能被转变为化学能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com