
| A.5.1g | B.10.2g | C.13.6g | D.15.3g |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.0. 06mol | B.0. 05mol | C.0.08mol | D.0.09mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
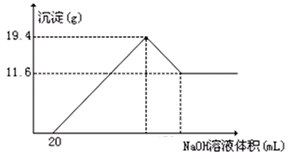
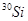 的原子的中子数为_________;
的原子的中子数为_________;查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.少量过氧化钠投入AlCl3溶液 | B.FeCl3溶液与NaHCO3溶液混合加热 |
| C.Ba(OH)2溶液与(NH4)2SO4 | D.明矾溶液与小苏打溶液混合 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
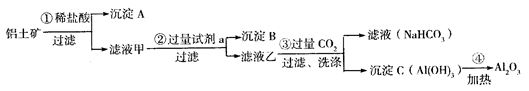
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 770 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1∶1 | B.3∶2 | C.2∶3 | D.1∶6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com