
 +2FeS+SO2,若CuFeS2中Cu、Fe的化合价都为+2,下列说法正确的是( )
+2FeS+SO2,若CuFeS2中Cu、Fe的化合价都为+2,下列说法正确的是( )| A、方框中的物质是Cu2S |
| B、CuFeS2仅作还原剂 |
| C、SO2既是氧化产物,又是还原产物 |
| D、若有1mol O2参加反应,则反应中有4mol电子转移 |


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
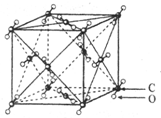 如图为干冰及其晶体的结构模型,下列有关分析正确的是( )
如图为干冰及其晶体的结构模型,下列有关分析正确的是( )| A、构成干冰的微粒是C原子和O原子 |
| B、CO2为极性分子 |
| C、干冰溶于水时有共价键要生成 |
| D、干冰中只存在微弱的分子间作用力 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 操作 | 选用仪器 |
| A | 称取3g左右的干海带 | 托盘天平 |
| B | 灼烧干海带至完全变成灰烬 | 烧杯 |
| C | 过滤煮沸后的海带灰与水的混合液 | 漏斗 |
| D | 用四氯化碳从氧化后的海带灰浸取液中提取碘 | 分液漏斗 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、体积②>③>① |
| B、物质的量 ②>③>① |
| C、质量③>②>① |
| D、氢原子个数③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H2>△H1 |
| B、△H1>△H2 |
| C、△H1=△H2 |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 | B、2:1 |
| C、3:1 | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molH2O含有6.02×1023个分子 |
| B、0.012Kg12C中含有6.02×1023个碳原子 |
| C、1molH2O中含有2 mol氢和1mol氧 |
| D、1molH2O中含有3 mol原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、150mL 3mol/L的CaCl2溶液 |
| B、75mL 1.5mol/L的MgCl2溶液 |
| C、50mL 1 mol/L的FeCl2溶液 |
| D、225mL 2mol/L的NH4Cl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com