
 灵星计算小达人系列答案
灵星计算小达人系列答案科目:高中化学 来源:2016届重庆市高三上学期第三次月考理综化学试卷(解析版) 题型:推断题
A、B、D、R、Q五种短周期主族元素,其原子序数依次增大,其中A原子核内无中子,B与D同周期,R与Q同周期,A与R同主族,D与Q同主族,D元素的原子最外层电子数是次外层电子数的三倍,B元素的最高正价和最低负价代数和为2。请用对应的化学用语回答下列问题:
(1)Q元素位于元素周期表中第______周期_____族。
(2)D、R、Q三种元素形成的简单离子的半径由大到小的顺序是________(用离子符号表示)。
(3)由A、B两种元素以原子个数比为5:1形成的离子化合物X,X的电子式为_______。
(4)由A、B元素形成的A2B4可以与O2、KOH溶液形成原电池,该原电池负极的电极反应式为____。
(5)由A、D、R、Q四种元素形成的化合物Y(RAQD3)(已知A2QD3的Ka1=1.2×10-2、Ka2=6.3×10-8),则Y溶液中各离子浓度由大到小的顺序为_______________;室温下,向Y溶液中加入一定量的NaOH,使溶液中c(AQD3-)=c(QD32-),则此时溶液呈______(填“酸性”、“碱性”或“中性”)
(6)Fe与D元素可形成Fe2D3、Fe3D4等化合物。向5.2g Fe2D3、Fe3D4、Cu的混合中加入0.5mol/L的硫酸溶液140mL时,固体恰好完全溶解,所得溶液中不含Fe3+。若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为______g。
查看答案和解析>>
科目:高中化学 来源:2016届云南省高三上第四次月考理综化学试卷(解析版) 题型:实验题
合成氨反应是化学上最重要的反应:
(1)合成氨原料气中的氢气可利用天然气(主要成分为CH4)在高温、催化剂作用下与水蒸气反应制得,反应中每生成2 mol CO2吸收316kJ热量,该反应的热化学方程式是_______________________,该方法制得的原料气中主要杂质是CO2,若用K2CO3溶液吸收,该反应的离子方程式是________________。
(2)已知N2(g)+3H2(g) 2NH3(g) ΔH<0。下图是当反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃下,反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线。
2NH3(g) ΔH<0。下图是当反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃下,反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线。
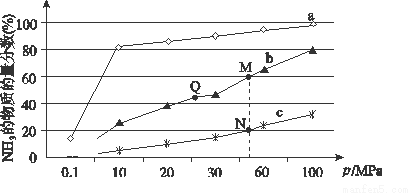
①曲线a对应的温度是________。
②关于工业合成氨的反应,下列叙述正确的是________(填序号)
A.上图中M、N、Q点平衡常数K的大小关系为K(M)=K(Q) >K(N)
B.加催化剂能加快反应速率但H2的平衡转化率不变
C.相同压强下,投料相同,达到平衡消耗时间关系为c>b>a
D.由曲线a可知,当压强增加到100 MPa以上,NH3的物质的量分数可达到100%
③N点时c(NH3)=0.2 mol·L-1,N点的化学平衡常数K=_________________(精确到小数点后两位)。
(3)合成氨工业中含氨废水的处理方法之一是电化学氧化法,将含氨的碱性废水通入电解系统后,在阳极上氨被氧化成氮气而脱除,阳极的电极反应式为______________________。
(4)NH3 可以处理NO2 的污染,方程式如下: NO2+ NH3 N2+ H2O(未配平)当转移0.6 mol电子时,消耗的NO2在标准状况下是 L。
N2+ H2O(未配平)当转移0.6 mol电子时,消耗的NO2在标准状况下是 L。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高一上半期测试化学试卷(解析版) 题型:选择题
将下列各组物质按酸、碱、盐分类依次排列,正确的是
A.硫酸、纯碱、小苏打 B.磷酸、熟石灰、苛性钠
C.硫酸氢钠、生石灰、醋酸钠 D.硫酸、烧碱、胆矾
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南省高二上12月段考化学试卷(解析版) 题型:选择题
有一处于平衡状态的反应:X(g)+3Y(g) 2Z(g) △H<0,为了使平衡向生成Z的方向移动,应选择的条件是
2Z(g) △H<0,为了使平衡向生成Z的方向移动,应选择的条件是
①高温 ②低温 ③高压 ④低压 ⑤加催化剂 ⑥分离出Z
A.①③⑤ B.②③⑤ C.②④⑥ D.②③⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:推断题
A、B、C、D、E代表五种常见元素,它们的核电荷数依次增大。其中元素E的基态3d轨道上有2个电子,A的基态原子L层电子数是K层电子数的2倍, B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物。请回答下列问题:
(1)E的基态原子价层电子排布式为_______________________________。
(2)AB2分子中,A的杂化类型为_______________________________。
(3)AB2形成的晶体的熔点________(填“大于”、“小于”或“无法判断”)CD形成的晶体的熔点,原因是_________________________。
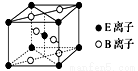
(4)E与B形成的一种橙红色晶体晶胞结构如图所示,其化学式为_______(用元素符号表示)。
(5)由C、D两元素形成的化合物组成的晶体中,阴、阳离子都具有或近似具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如图所示为C、D形成化合物的晶胞结构图以及晶胞的剖面图:
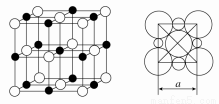
若a=5.6×10-8 cm,则该晶体的密度为________g·cm-3(精确到小数点后1位)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
下列各组物质中,按熔点由低到高的顺序排列正确的是( )
①Na、K、Rb ②CO、KCl、SiO2 ③O2、I2、Hg ④Na、Mg、Al
A.①③ B.①④ C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二上期中测试化学试卷(解析版) 题型:选择题
13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,Kurt Wu thrich等人为此获得2002年诺贝尔化学奖。下列有关13C、15N叙述正确的是
A.13C与15N有相同的中子数
B.13C与C60互为同素异形体
C.15N与14N互为同位素
D.15N的核外电子数与中子数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com