
| A. | ①② | B. | ②③ | C. | ①②③ | D. | 全部 |
分析 ①NH4H是铵根离子与氢负离子通过离子键形成的离子化合物;
②NH4H溶于水生成NH3•H20和H2;
③根据H元素的化合价变化判断;
④NH4H固体投入少量的水中,生成氨水和氢气,NH3•H2O分解为NH3和H2O.
解答 解:①NH4H与氯化铵的结构相似,是由NH4+和H-构成的离子化合物,含有离子键和共价键,故①正确;
②NH4H与水反应有H2和氨气生成,溶液呈碱性,故②错误;
③NH4H与水发生了氧化还原反应,氢负离子化合价升高,被氧化,做还原剂,故③错误;
④NH4H固体投入少量的水中生成氨水和氢气,由于发生的氧化还原反应是放热的,生成的NH3•H2O分解为NH3和H2O,所以可以得到两种气体,故④正确;
故选:B.
点评 本题考查了铵盐的结构和性质,侧重氧化还原反应迁移应用能力的考查,明确反应中元素的化合价变化为解答的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1 | B. | 0.2mol•L-1 | C. | 0.5mol•L-1 | D. | 1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16g CH4中含有4NA个C-H键 | |
| B. | 1L mol•L-1CH3COOH溶液中含有0.1NA个H+ | |
| C. | 标准状况下的22.4L辛烷完全燃烧,生成CO2分子数为8NA | |
| D. | 1mol 乙炔中含有的电子数为12NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
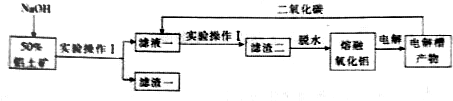
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子的球棍模型: | B. | NH4Cl的电子式: | ||
| C. | F原子的结构示意图: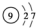 | D. | 中子数为20的氯原子${\;}_{17}^{37}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,2.24LSO2所含有的分子数小于0.1NA | |
| B. | 1L 1 mol•L-1 FeCl3溶液完全水解产生的Fe(OH)3胶体粒子数为NA | |
| C. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| D. | 28.6gNa2CO3•10H2O溶于水配成1L溶液,该溶液中阴离子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)3 C-CH=CH2 | B. | CH3CH=C(CH3)C (CH3)3 | ||
| C. | HC≡CCH(CH3)C(CH3)3 | D. | (CH3)3CC(CH3)=CHCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
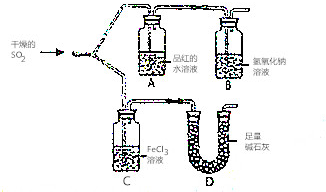 如图装置进行SO2气体性质实验
如图装置进行SO2气体性质实验查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com