
| A、Ba2+、Na+、NO3-、Cl- |
| B、Ca2+、Na+、Fe3+、SO32- |
| C、K+、OH-、HCO3-、NO3- |
| D、Mg2+、Cl-、Al3+、SO42- |


科目:高中化学 来源: 题型:
| A、火碱、烧碱、生石灰 |
| B、生石灰、冰、干冰 |
| C、熟石灰、苛性钠、氢氧化钾 |
| D、纯碱、硫酸钠、胆矾 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A. | 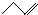 |
丁烯 |
| B. | 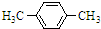 |
对二甲苯 |
| C. | 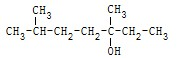 |
2,5-二甲基-5-庚醇 |
| D. | CH3CH(C2H5)CH(CH3)2 | 2,3-二甲基戊烷 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应中既有物质变化又有能量变化 |
| B、即使没有发生化学变化,也可能有能量的变化 |
| C、任何化学反应中的能量变化都表现为热量变化 |
| D、物质的化学能可以通过不同的变化方式转化为热能、电能等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用石灰石(CaCO3)与盐酸反应制CO2:CO32-+2H+=H2O+CO2↑ |
| B、用FeCl3溶液溶解单质Fe:Fe3++Fe=2Fe2+ |
| C、用氢氧化钠溶液吸收氯气:Cl2+2OH-=Cl-+ClO-+H2O |
| D、AlCl3溶液与氨水(过量)混合:Al3++4NH3﹒H2O=AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CHCl3+HF→CHFCl2+HCl | ||
| B、CH2=CH2+H2O→CH3CH2OH | ||
| C、CH≡CH+2Br2→CHBr2-CHBr2 | ||
D、CH4
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 4 |
| A、(1)、(4) |
| B、只有(3) |
| C、只有(2) |
| D、(1)(2)(3)(4) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应中CCl4为氧化剂 |
| B、金刚石属于金属单质 |
| C、CCl4是一种有机化合物 |
| D、该反应属于置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
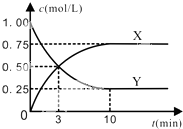 在一恒温、恒容密闭容器中充入1mol CO2和3mol H2,一定条件下发生反应:
在一恒温、恒容密闭容器中充入1mol CO2和3mol H2,一定条件下发生反应:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com