
 如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )| 选项 | a | b | c |
| A | Fe | FeCl3 | FeCl2 |
| B | HCl | Cl2 | HClO |
| C | H2SO4 | SO2 | SO3 |
| D | CH2=CH2 | CH3CH2OH | CH3CHO |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Fe与氯气反应生成氯化铁,氯化铁和Fe反应生成氯化亚铁,Zn与氯化亚铁反应生成Fe;
B.氯气被氧化生成氯气,氯气和水反应生成HClO,HClO分解生成HCl;
C.硫酸可被还原生成二氧化硫,二氧化硫氧化生成三氧化硫、三氧化硫和水反应生成硫酸;
D.乙醛不能生成乙烯.
解答 解:A.Fe与氯气反应生成氯化铁,氯化铁和Fe反应生成氯化亚铁,Zn与氯化亚铁反应生成Fe,符合上述转化关系,故A不选;
B.氯气被氧化生成氯气,氯气和水反应生成HClO,HClO分解生成HCl,能实现如图所示转化,故B不选;
C.硫酸可被还原生成二氧化硫,二氧化硫氧化生成三氧化硫、三氧化硫和水反应生成硫酸,能实现如图所示转化,故C不选;
D.乙烯可生成乙醇,乙醇被氧化生成乙醛,但乙醛不能生成乙烯,故D选.
故选D.
点评 本题考查物质的性质及相互转化,综合考查元素化合物知识,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是由26个原子构成的物质 | B. | 氮元素的质量分数为17.3% | ||
| C. | C、H、O 元素的质量比为10:14:2 | D. | 相对分子质量是162g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
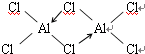 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
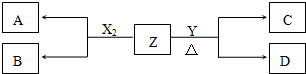
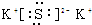 ,D的水溶液pH>7(填“=”、“>”或“<”.
,D的水溶液pH>7(填“=”、“>”或“<”.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 李比希燃烧法、钠熔法、铜丝燃烧法都是用来分析有机物元素组成的方法 | |
| B. | 红外光谱法、紫外光谱法、核磁共振、质谱仪等都是现代化学测定有机物结构的常用方法 | |
| C. | 同位素示踪法是研究化学反应历程的手段之一 | |
| D. | CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H-NMR 谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用1H-NMR 来鉴别 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com