
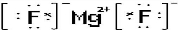 .
.分析 有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A的原子核无中子,则A为H,能与B、C分别形成10电子的化合物,B、C的族序数为奇数,则B为N,C为F,B、C的质子数之和与E的质子数相等,则E为S,D、E位于同一周期,D的阳离子所带的正电荷数等于该阳离子的电子层数,则D为Mg,据此答题.
解答 解:有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A的原子核无中子,则A为H,能与B、C分别形成10电子的化合物,B、C的族序数为奇数,则B为N,C为F,B、C的质子数之和与E的质子数相等,则E为S,D、E位于同一周期,D的阳离子所带的正电荷数等于该阳离子的电子层数,则D为Mg,
(1)C与D形成的化合物为MgF2,其电子式为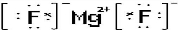 ,
,
故答案为: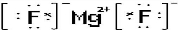 ;
;
(2)Mg与CO2反应的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO,
故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO;
(3)“嫦娥一号”发射所用的液体燃料是氢元素的单质,
故答案为:氢;
(4)工业上,使二氧化硫转化为三氧化硫的设备名称为接触室,
故答案为:接触室;
(5)在一定的条件下,H2、N2混合物经过一段时间的反应后,N2的浓度减小了0.3mol/L.此时间内H2表示的化学反应速率为0.45mol/(L•s),则用N2表示的化学反应速率为0.15mol/(L•s),根据t=$\frac{△c}{v}$可知,此段反应时间为$\frac{0.3mol/L}{0.15mol/(L•s)}$=2s,
故答案为:2.
点评 本题主要考查的是元素的推断,涉及知识点:电子式书写、化学方程式书写、化学工业、反应速率的应用等,有一定的综合性,题目难度中等.


 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:多选题
| A. | 水、汽油、酒精 | B. | AgNO3、NaOH、KI | C. | NaCl、NaBr、NaI | D. | 汽油、酒精、NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
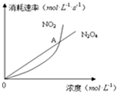 在80℃时,将0.40mol 的N2O4气体充入2L 已经抽成真空的固定容积的密闭容器中,发生如下反应:N2O4(g)?2NO2(g)△H=+56.9kJ/mol,隔一段时间对该容器内的物质进行分析,得到如下数据:
在80℃时,将0.40mol 的N2O4气体充入2L 已经抽成真空的固定容积的密闭容器中,发生如下反应:N2O4(g)?2NO2(g)△H=+56.9kJ/mol,隔一段时间对该容器内的物质进行分析,得到如下数据:| 时间/s n/mol | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一种元素可能形成多种氧化物,但同价态的氧化物只有一种 | |
| B. | 明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 | |
| C. | 已知K2O、K2O2、KO2的名称依次是氧化钾、过氧化钾、超氧化钾,则BaO2的名称是过氧化钡 | |
| D. | 由共价键形成的物质一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解饱和氯化钠溶液:2Cl-+2H+ $\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑ | |
| B. | 用银氨溶液检验乙醛中的醛基: CH3CHO+2Ag(NH3)2++2OH-$\stackrel{水浴加热}{→}$CH3COONH4+3NH3+2Ag↓+H2O | |
| C. | Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-═5SO42-+2Mn2+ 3H2O | |
| D. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铵与氢氧化钠两种稀溶液混合:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$H2O+NH3↑ | |
| B. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| C. | 氢氧化镁与稀硫酸反应:H++OH-=H2O | |
| D. | 单质铜与稀硝酸反应:Cu+2H++2NO3-=Cu2++2NO↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素在人体内可水解为葡萄糖,故可作人类的营养物质 | |
| B. | 鱼虾会产生不愉快的腥臭味,可在烹调时加入少量食醋和料酒 | |
| C. | 被蜂蚁蜇咬会感觉疼痛难忍,这是由于人的皮肤被注入了甲酸的缘故,此时若能涂抹稀氨水或碳酸氢钠溶液,可以减轻疼痛 | |
| D. | 苯酚溶液可用于环境消毒,医用酒精可用于皮肤消毒,其原因均在于可使蛋白质变性凝固 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com