
| 方案序号 | 分析 | 误差(偏低或偏高) | 改变措施 |
| | | | |
| | | | |
| | | | |
| | | | |
 (2分)
(2分) CuSO4 + SO2↑+ 2H2O(2分)
CuSO4 + SO2↑+ 2H2O(2分)| 方案序号 | 分析 | 误差(偏低或偏高) | 改变措施 |
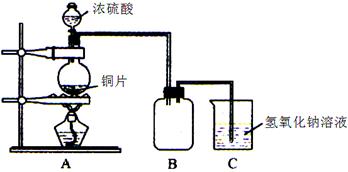
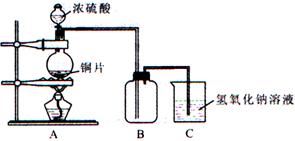
| A | 碱石灰除吸收二氧化硫外还能吸收水,测得二氧化硫质量增大 | 偏低 | A产生的气体先经浓硫酸干燥,后用碱石灰吸收 |
| B | 高锰酸钾溶液中含有硫酸,与氯化钡反应生成沉淀增大 | 偏低 | 将硫酸酸化的高锰酸钾溶液换成溴水或碘水或硝酸溶液 |
| C | 二氧化硫在水中以1∶40溶解,收集二氧化硫体积减少 | 偏高 | 将水换成四氯化碳、煤油等非极性溶剂 |
| D | 亚硫酸钡在空气中烘干及称重过程中部分被氧化生成硫酸钡,产生固体质量增大 | 偏低 | 先将二氧化硫用强氧化剂如溴水氧化,再加入足量的氯化钡溶液或氢氧化钡溶液 |


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
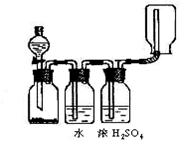
| A.⑥⑤④①③② | B.⑥④⑤②①③ | C.⑥④①③⑤② | D.②⑥④①③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.实验室制取乙烯的反应原理:C2H5OH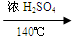 C2H4 ↑+ H2O C2H4 ↑+ H2O |
| B.实验室制取C2H2,一般用碳化钙跟饱和食盐水反应以适度减缓反应速率 |
| C.实验室分离苯和苯酚的混合物,可采用溴水 |
| D.由1—溴丁烷跟氢氧化钠醇溶液共热,可以制得两种烯烃 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
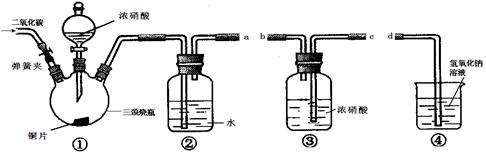
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.偏低l% | B.偏高1% | C.无影响 | D.偏高0.1% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 +8H2O
+8H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com