
【题目】人类很早就懂得使用铁器,如今对铁元素的研究依然热度不减。请回答:
(1)铁原子L能层上有__________种不同运动状态的电子,基态铁原子的外围电子排布式为_____________。
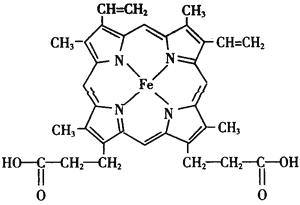
(2)血红素是血液的重要组成部分,其结构如图。其中C原子和N原子具有的相同的杂化方式为________________,N与Fe之间存在的相互作用是___________。血红素在人
体内合成时的基本原料之一是甘氨酸(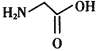 ),其分子中σ键和π键的个数比为___________。
),其分子中σ键和π键的个数比为___________。
(3)单质铁的某种晶体拥有体心立方晶胞,其配位数为___________,若其晶胞边长为a pm,其晶体密度为___________g/cm3(用含a的代数式表示,NA表示阿伏加德罗常数)。
(4)铁氰化钾(K3)俗称赤血盐,可用于检验Fe2+,反应的离子方程式为_____________。其配体的电子式为_______________,与其配体互为等电子体的微粒有_____________(任写两种,填化学式)。
【答案】 8 3d64s2 sp2、sp3 极性键、配位键 9:1 8 ![]() 3Fe2+ +2 3- =Fe32↓
3Fe2+ +2 3- =Fe32↓ ![]() N2、C22-、CO等
N2、C22-、CO等
【解析】(1)铁的电子排布式为1s22s22p63s23p63d64s2,L能层为2s22p6,有8种不同运动状态的电子,基态铁原子的外围电子排布式为3d64s2;
(2)根据每个N原子含有的σ 键个数与孤电子对数之和判断其杂化方式;血红素中N原子有的含有3个σ 键和一个孤电子对,属于sp3杂化;有的含有3个σ 键,属于sp2 杂化方式;N与Fe之间存在的相互作用是极性键、配位键;甘氨酸(![]() ),其分子中σ键和π键的个数比为9∶1;
),其分子中σ键和π键的个数比为9∶1;
(3)根据晶胞中的配位情况,一个晶胞中含有2个铁,1pm=10-10cm,由ρ=![]() =
=![]() =
=![]() g/cm3;
g/cm3;
(4)铁氰化钾(K3[Fe(CN)6])俗称赤血盐,可用于检验Fe2+,反应的离子方程式为 3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓;其配体为CN-,它的电子式为![]() ;等电子体为电子数相等,原子数也相等,与其配体互为等电子体的微粒有N2、CO。
;等电子体为电子数相等,原子数也相等,与其配体互为等电子体的微粒有N2、CO。


科目:高中化学 来源: 题型:
【题目】铁和铜都是日常生活中常见的金属,有着广泛的用途。请回答下列问题:
(1)铁在元素周期表中的位置_________。
(2)配合物Fe(CO)n常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)n晶体属于______(填晶体类型)。Fe(CO)n的中心原子价电子数与配体提供电子数之和为18,则n=______ 。Fe(CO)n在一定条件下发生反应:Fe(CO)n(s)![]() Fe(s)+ n CO(g)。已知反应过程中只断裂配位键,则该反应生成物中新形成的化学键类型为___________。
Fe(s)+ n CO(g)。已知反应过程中只断裂配位键,则该反应生成物中新形成的化学键类型为___________。
(3)K3[Fe(CN)6]溶液可用于检验________(填离子符号)。CN-中碳原子杂化轨道类型为_________,C、N、O三元素的第一电离能由大到小的顺序为_______(用元素符号表示)。
(4)铜晶体的晶胞如右图所示。
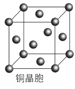
①基态铜原子的核外电子排布式为________________。
②每个铜原子周围距离最近的铜原子数目________。
(5)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如附图所示(黑点代表铜原子)。
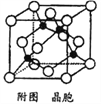
①该晶体的化学式为____________。
②已知该晶体的密度为g.cm-3,阿伏伽德罗常数为NA,则该晶体中铜原子和M原子之间的最短距离为_________pm(只写计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电解质溶液有关叙述正确的是
A.恒温条件下稀释氢氟酸时,HF的Ka增大,水的KW不变
B.向Mg(OH)2沉淀悬浊液中加入NH4Cl固体,c(Mg2+)、c(OH-)浓度均增大
C.0.1mol/LNaHCO3溶液中,c(Na+)>c(![]() )>c(
)>c(![]() )>c(H2CO3)
)>c(H2CO3)
D.0.1mol/LNa2SO3溶液中,加入少量NaOH固体,c(![]() )与c(Na+)均增大
)与c(Na+)均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的应用错误的是
A.可用氧化铁与铝在高温下反应炼铁B.硫化钠与浓硫酸反应可制备硫化氢
C.铁丝在氯气中燃烧可制得无水三氯化铁D.氧化钙与水反应可用作自热米饭加热
查看答案和解析>>
科目:高中化学 来源: 题型:
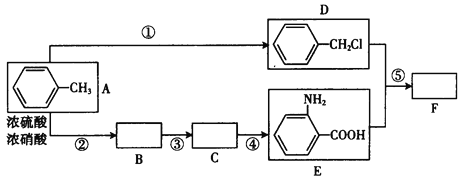
【题目】化合物F是用于制备药品盐酸祛炎痛的中间产物,已知其合成路线如下:
Ⅰ.RNH2+![]() CH2Cl
CH2Cl![]() RNHCH2
RNHCH2![]() +HCl(R和
+HCl(R和![]() 代表烃基)
代表烃基)
Ⅱ.苯的同系物易被高锰酸钾溶液氧化如下:
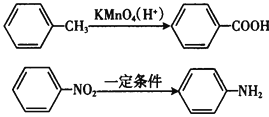
Ⅲ.苯胺具有弱碱性,易氧化。
回答下列问题:
(1)写出反应①的反应物质和条件_____________,B中所含官能团的名称_____________,C的结构简式__________________。
(2)D+E→F的化学方程式:______________。
(3)E的一种同分异构体(对位氨基)在一定条件下,可聚合成热固性很好的功能高分子,写出合成此高聚物的化学方程式__________________。
(4)写出D的含有苯环的同分异构体,已知该核磁共振氢谱图有3种不同类型的氢原子,峰面积之比为3 :2 :2,则该物质是______________(写结构简式)。
(5)反应①~⑤中,属于取代反应的是(填反应序号)________________,反应③的反应类型_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲苯(![]() )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛(![]() )、苯甲酸(
)、苯甲酸(![]() )等产品。下表列出了有关物质的部分物理性质,请回答:
)等产品。下表列出了有关物质的部分物理性质,请回答:
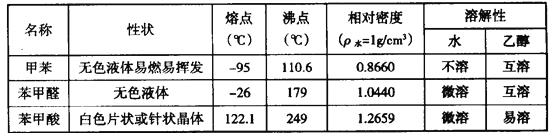
注:甲苯、苯甲醛、苯甲酸三者互溶; 酸性: 苯甲酸>醋酸
实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸和2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时。
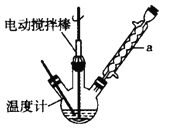
(1)装置a的名称是____ ____,主要作用是 。三颈瓶中发生反应的化学方程式为 ,此反应的原子利用率理论上可达 。
(2)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是________________。
(3)反应完毕后,反应混合液经过自然冷却至室温时,还应经过________、________(填操作名称)等操作,才能得到苯甲醛粗产品。
(4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸。
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是_______(按步骤顺序填字母)。
a.对混合液进行分液 b.过滤、洗涤、干燥
c.水层中加入盐酸调节pH=2 d.与适量碳酸氢钠溶液混合震荡
②若对实验①中获得的苯甲酸产品进行纯度测定,可称取1.200g产品,溶于100mL乙醇配成溶液,量取所得的乙醇溶液20.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000mol/L KOH标准液滴定,到达滴定终点时消耗KOH溶液18.00mL。产品中苯甲酸的质量分数为________。
③下列情况会使测定结果偏低的是__________(填字母)。
a.滴定终点时俯视读取耗碱量 b.KOH标准液长时间接触空气
c.配制KOH标准液时仰视定容 d.将酚酞指示剂换为甲基橙溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4的主要流程如下:
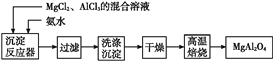
(1)制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式为_____________。
(2)判断流程中沉淀是否洗净所用的试剂是__________________。
(3)在25 ℃下,向浓度均为0.01 mol·L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成______沉淀(填化学式),生成该沉淀的离子方程式:_____________。{已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10-34}。
(4)无水AlCl3(183 ℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
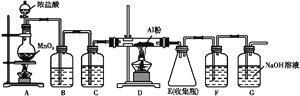
装置B中盛放饱和NaCl溶液,该装置的主要作用是______;F中试剂的作用是__________________________________________。
(5)将Mg、Cu组成的3.92 g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体1.792 L(标准状况),向反应后的溶液中加入4 mol·L-1的NaOH溶液80 mL时金属离子恰好完全沉淀。则形成沉淀的质量为____g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com