

| A. | 三聚氰胺的分子式为C3H6N6 | |
| B. | 三聚氰胺分子中的所有原子均位于同一平面上 | |
| C. | 三聚氰胺的一取代物只有一种 | |
| D. | 三聚氰胺不属于芳香烃 |
分析 A.根据结构判断含有的元素种类和原子个数,可确定分子式;
B.氨基中的原子不会在同一平面上;
C.三聚氰胺结构对称,只有一种H原子;
D.含有苯环的烃属于芳香烃,且在元素组成上只含有C、H两种元素.
解答 解:A.由三聚氰胺的分子结构图可知,1个三聚氰胺分子是由3个碳原子、6个氢原子、6个氮原子构成的,其化学式为C3H6N6,故A正确;
B.在三聚氰胺中,氨基中的N、H原子不会在同一平面上,故B错误;
C.三聚氰胺结构对称,只有一种H原子,一取代物只有一种,故C正确;
D.三聚氰胺中不含有苯环,在元素组成上含有C、H、N三种元素,不属于芳香烃,故D正确;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重物质组成和二氯取代物的考查,注意结构对称性,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | N2→NH3→NO→NO2→HNO3 | B. | Na→Na2O2→NaOH→Na2CO3 | ||
| C. | S→SO3→H2SO4→Na2SO4 | D. | Si→SiO2→Na2SiO3→H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2S与SO2、NO与O2、NH3与HCl在常温下均不能大量共存 | |
| B. | (NH4)2SO3、Ca(ClO)2、NaAlO2均既能和稀硫酸又能和氢氧化钠溶液反应 | |
| C. | Fe(OH)3、FeCl2、FeCl3、NO均可通过化合反应得到 | |
| D. | AlCl3、Fe3O4、NaOH都可通过置换反应一步得到也可通过化合反应一步得到 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体 | |
| B. | 用氢氧化钠溶液鉴别Al2(SO4)3和 MgSO4两种无色溶液 | |
| C. | 用焰色反应实验来鉴别NaNO3固体和 KNO3固体 | |
| D. | 用澄清石灰水鉴别碳酸钠和碳酸氢钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用NaOH溶液鉴别(NH4)2SO4和NH4Cl | |
| B. | 用AgNO3溶液鉴别NaBr溶液和KI溶液 | |
| C. | 用焰色反应鉴别NaCl和NaNO3 | |
| D. | 用澄清石灰水鉴别CO2和SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23gNa在氧气中完全燃烧失电子数为0.5NA | |
| B. | 1mol NO和1mol O2的混合气体中含有的分子数为2NA | |
| C. | 标准状况下,11.2L SO3所含分子数为0.5NA | |
| D. | 1.5mol NO2与足量H2O反应,转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO的燃烧热为566 kJ/mol | |
| B. | 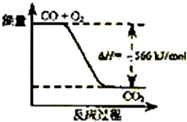 如图可表示由CO生成CO2的反应过程和能量关系 | |
| C. | 2Na2O2(s)+2CO2(s)═2Na2CO3(s)+O2(g)△H<-452 kJ/mol | |
| D. | CO2(g)与Na2O2(s)反应放出452kJ热量时,电子转移数为4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com