
下列叙述能肯定金属A 比金属B更活泼的是
A.A原子的最外层电子数比B原子的最外层电子数少
B.A原子的电子层数比B原子多
C.1 mol A从酸中置换出H2比1 mol B多
D.常温下,A能从酸中置换出氢气,而B不能
科目:高中化学 来源: 题型:
下列说法不正确的是( )
 A.室温下,44g乙醛和乙酸乙酯的混合物中含有的碳原子数目为2NA
A.室温下,44g乙醛和乙酸乙酯的混合物中含有的碳原子数目为2NA
 B.标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA
B.标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA
 C.食醋中含有乙酸,乙酸可由乙醇连续氧化得到
C.食醋中含有乙酸,乙酸可由乙醇连续氧化得到
 D.煤可与水蒸气反应制成水煤气,水煤气的主要成分为CO和H2
D.煤可与水蒸气反应制成水煤气,水煤气的主要成分为CO和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
某含氧有机化合物,它的相对分子质量为88.0,含C的质量分数为68.2%,含H的质量分数为13.6%,经红外光谱测定含有一个羟基,核磁共振氢谱显示该分子中有3个甲基,且有三种不同环境的氢原子,请通过计算写出其结构简式。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的 (同温同压),这时混合气体中N2、O2、CO2物质的量之比为 ( )
(同温同压),这时混合气体中N2、O2、CO2物质的量之比为 ( )
A. 3∶4∶1 B. 3∶3∶2 C. 6∶7∶3 D. 6∶9∶0
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示物质结构的化学用语或模型正确的是
A.二氧化碳的结构式: O=C=O B.HF的电子式:
C.Cl-离子的结构示意图: D.CH4分子的球棍模型:
D.CH4分子的球棍模型:
查看答案和解析>>
科目:高中化学 来源: 题型:
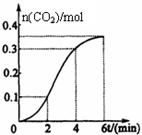
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如右图所示。下列结论不正确的是
A.反应开始2分钟内平均反应速率最大
B.反应4分钟后平均反应速率最小
C.反应开始4分钟内温度对反应速率的影响比浓度大
D.反应4分钟后反应速率下降的原因是盐酸浓度逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)X元素是 (填名称) ,W在周期表中的位置 。
(2)X与Y 形成化合物的电子式为 ,X与W组成的化合物中存在 键(填“离子”“共价”)。
(3)①写出实验室制备YX3的化学方程式:
②工业上也可以选择合适的条件进行YX3的合成,若已知在该条件下每生成2 mol YX3气体时放出
92.4kJ的热量,写出该反应的热化学方程式
(4)由X、Y、Z、W四种元素组成的一种离子化合物A。已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。则A的名称是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
以粗氧化锌粉(含FeO、Fe2O3、ZnS等)制取活性ZnO的工艺如下:
步骤1:以H2SO4浸出粗氧化锌,同时加入H2O2;
步骤2:过滤,调节滤液的pH;
步骤3:过滤,向滤液中加NH4HCO3,得碱式碳酸锌沉淀;
步骤4:过滤、洗涤、煅烧,得产品。
已知:离子沉淀的pH见下表。
| 离子 | 开始沉淀pH | 沉淀完全pH |
| Fe2+ | 7.6 | 9.6 |
| Fe3+ | 2.7 | 3.7 |
| Zn2+ | 5.4 | 8.0 |
(1)加入H2O2时能浸出硫化锌,同时生成淡黄色固体,写出其化学方程式 ▲ 。
(2)步骤2中调节溶液pH的范围是 ▲ 。
(3)取洗涤、干燥后的碱式碳酸锌68.2 g,充分灼烧后测得残留物质的质量为48.6 g,将所得气体通入足量澄清石灰水中,得沉淀20 g。计算碱式碳酸锌的组成(用化学式表示,写出计算过程)。 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某原电池的总反应的离子方程式是Zn + Cu2+ = Zn2+ + Cu,该原电池的组成正确的是:
| A | B | C | D | |
| 正极 | Zn | Ag | Cu | Cu |
| 负极 | Cu | Cu | Zn | Zn |
| 电解质溶液 | CuCl2 | H2SO4 | CuSO4 | FeCl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com