
 新修改的《机动车驾驶证申领和使用规定》于2010年4月1日起实施,新规规定酒驾一次扣12分,出此拳治理酒驾是因酒后驾车是引发交通事故的重要原因.如图所示为交警在对驾驶员是否饮酒进行检测.其原理是:橙色的酸性K2Cr2O7水溶液遇呼出的乙醇蒸气迅速变蓝,生成蓝绿色的Cr3+.下列对乙醇的描述与此测定原理有关的是( )
新修改的《机动车驾驶证申领和使用规定》于2010年4月1日起实施,新规规定酒驾一次扣12分,出此拳治理酒驾是因酒后驾车是引发交通事故的重要原因.如图所示为交警在对驾驶员是否饮酒进行检测.其原理是:橙色的酸性K2Cr2O7水溶液遇呼出的乙醇蒸气迅速变蓝,生成蓝绿色的Cr3+.下列对乙醇的描述与此测定原理有关的是( )| A. | ②⑤ | B. | ②③ | C. | ①③ | D. | ①④ |
分析 根据乙醇沸点低,易挥发,故可以易被检测及乙醇具有还原性,K2Cr2C7具有强氧化性,可以氧化乙醇,自身生成Cr3+来分析解答.
解答 解:①乙醇沸点低,易挥发,可以易被检测,与测定原理有关;
②乙醇密度比水小,可与水以任意比混溶,与测定原理无关;
③乙醇分子中含有羟基,具有还原性,K2Cr2C7具有强氧化性,可以把乙醇迅速氧化为乙酸蓝绿色的Cr3+,与测定原理有关;
④乙醇可看成是乙烷中的氢原子被羟基取代后的产物,是烃的含氧化合物,与测定原理无关;
⑤乙醇可与羧酸在浓硫酸的作用下发生取代反应,与测定原理无关;
对乙醇的描述与此测定原理有关的是①③.
故选C.
点评 本题考查了乙醇的性质,要根据用途进行选择合理答案,本题中的信息交警对驾驶员进行呼气酒精检测的原理是解答的关键,学生应学会信息的抽取和应用来解答习题.


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)中一种重要的掺杂剂.实验室要用黄磷(白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如下图所示:(部分夹持装置略去)
半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)中一种重要的掺杂剂.实验室要用黄磷(白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如下图所示:(部分夹持装置略去)| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| PCl5 | 2 | 105.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2-酸性氧化物 Na2O2-碱性氧化物 Al2O3-两性氧化物 | |
| B. | 漂白粉-混合物 胆矾-纯净物 HD-单质 | |
| C. | 纯碱-碱 硫化氢-酸 小苏打-酸式盐 | |
| D. | 盐酸-强电解质 硫酸钡-强电解质 醋酸-弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
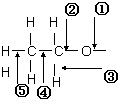 乙醇分子中各化学键如图所示:
乙醇分子中各化学键如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com