
常温下硫单质主要以S8形式存在,加热时S8会转化为S6、S4、S2等,当蒸气温度达到750°C时主要以S2形式存在,下列说法正确的是( )
| A.S8转化为S6、S4、S2属于物理变化 |
| B.不论哪种硫分子,完全燃烧时都生成SO2 |
| C.常温条件下单质硫为原子晶体 |
| D.把硫单质在空气中加热到750°C即得S2 |
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:单选题
关于离子键、共价键的各种叙述中正确的是( )
| A.在离子化合物里,只存在离子键,没有共价键 |
| B.非极性键只存在于双原子的单质分子(如Cl2)中 |
| C.由不同元素组成的多原子分子里,一定只存在极性键 |
| D.共价化合物分子中,一定不存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
韩国首尔大学的科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成“暖冰”。则关于“暖冰”的判断正确的是
| A.“暖冰”中存在离子键 |
| B.“暖冰”中水分子的O-H键是非极性键 |
| C.“暖冰”的密度大,有导电性和导热性 |
| D.水凝固形成20℃时的“暖冰”所发生的变化是物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
以下有关杂化轨道的说法中错误的是( )
| A.ⅠA族元素成键时不可能有杂化轨道 |
| B.杂化轨道既可能形成σ键,也可能形成π键 |
| C.孤对电子有可能参加杂化 |
| D.s轨道和p轨道杂化不可能有sp4出现 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为( )
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道 |
| C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强 |
| D.以上说法都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知CO2、BF3、CH4、SO3都是非极性分子,NH3、H2S、H2O、SO2都是极性分子,由此可推知ABn型分子是非极性分子的经验规律是( )
| A.分子中所有原子在同一平面内 |
| B.分子中不含氢原子 |
| C.在ABn分子中,A元素为最高正价 |
| D.在ABn型分子中,A原子最外层电子都已成键 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用一带静电的玻璃棒靠近A、B两种纯液体流,根据图分析,这两种液体分子的极性正确的是( )。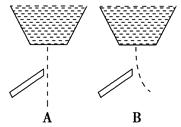
A.A是极性分子,B是非极性分子
B.A是非极性分子,B是极性分子
C.A和B都是极性分子
D.A和B都是非极性分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com