
| 成分 | 质量(g) | 摩尔质量(g?mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.316 | 158 |
| 硝酸银 | 0.075 | 170 |

| n |
| V |
| 0.87g |
| 174g/mol |
| 0.316g |
| 158g/mol |
| 0.012mol |
| 0.5L |


科目:高中化学 来源: 题型:
 往一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)?2HI(g);△H<0,当达到平衡后,t0时改变反应的某一条件,平衡图象如图,则下列说法正确的是( )
往一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)?2HI(g);△H<0,当达到平衡后,t0时改变反应的某一条件,平衡图象如图,则下列说法正确的是( )| A、容器内气体颜色变深,平均相对分子质量不变 |
| B、平衡不移动,混合气体密度增大 |
| C、H2转化率增大,HI平衡浓度变小 |
| D、t0时改变的条件是增压 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
| B、向碘水中通入SO2,碘水褪色说明SO2具有漂白性 |
| C、蘸有浓硫酸的玻璃棒接近浓氨水瓶口有白烟产生 |
| D、某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 的有机物可以通过不同的反应得到下列四种物质:
的有机物可以通过不同的反应得到下列四种物质: ②
② ③
③ ④X(C18H16O4)
④X(C18H16O4)查看答案和解析>>
科目:高中化学 来源: 题型:
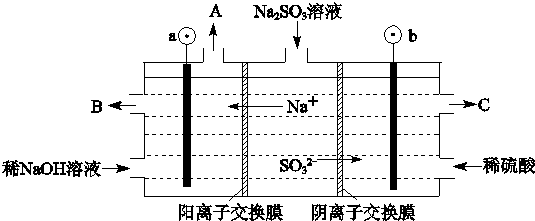
查看答案和解析>>
科目:高中化学 来源: 题型:
 .试回答:
.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com