
A.n=![]() B.a%=
B.a%=![]()
C.M=![]() D.S=
D.S=![]()
科目:高中化学 来源: 题型:
 (1)碳氢化合物完全燃烧生成CO2和H2O.常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol?L-1.若忽略水的电离及H2CO3的第二级电离,请计算可逆反应H2CO3
(1)碳氢化合物完全燃烧生成CO2和H2O.常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol?L-1.若忽略水的电离及H2CO3的第二级电离,请计算可逆反应H2CO3 HCO3-+H+的平衡常数K1.(已知10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1.(已知10-5.60=2.5×10-6)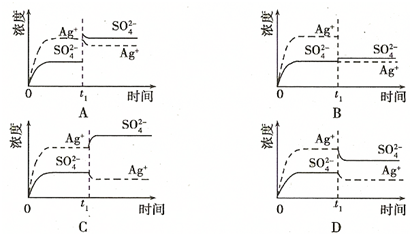
查看答案和解析>>
科目:高中化学 来源: 题型:
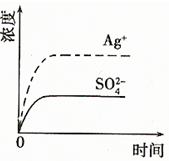
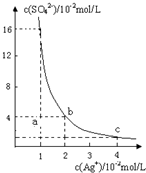 某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示:
某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
 (2008?广东)已知Ag2SO4的KW 为2.0×10-3,将适量Ag2SO4固体溶于100mL水中至刚好饱和,该过程中Ag+和S
(2008?广东)已知Ag2SO4的KW 为2.0×10-3,将适量Ag2SO4固体溶于100mL水中至刚好饱和,该过程中Ag+和S| O | 2- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、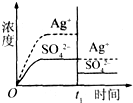 加入100mL蒸馏水 | B、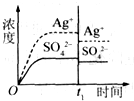 加入100mL 0.010mol?L-1 Ag2SO4 | C、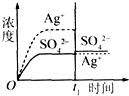 加入100mL 0.020mol?L-1 Na2SO4溶液 | D、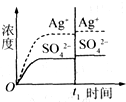 加入100mL 0.040mol?L-1 AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省高三12月联考化学试卷 题型:选择题
已知Ag2SO4的Ksp为2.0×10-5,将适量Ag2SO4固体溶于100 mL水中至刚好饱和, 该过程中Ag+和SO42-浓度随时间变化关系如右图(饱和Ag2SO4溶液中c(Ag+)=0.034 mol/L)。若t1时刻在上述体系中加入100 mL 0.020 mol/L Na2SO4溶液,下列示意图中,能正确表示t1时刻后Ag+和SO42-浓度随时间变化关系的是
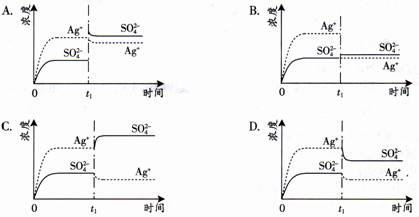
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com