
高分子材料PET聚酯树脂和PMMA的合成路线如下:
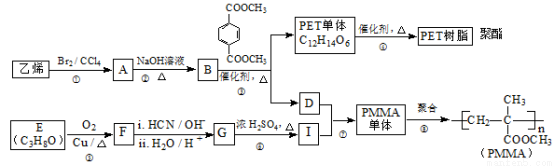
已知: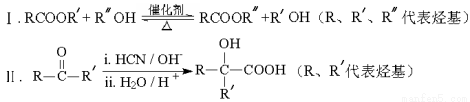
(1)①的反应类型是__________;③的反应类型是__________。
(2)②的化学方程式为_______________________________________________。
(3)PMMA单体的官能团名称是________、________。
(4)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为__________________________。
(5)I的结构简式为__________________。
(6)下列说法正确的是________(填字母序号)。
a. B和D互为同系物 b. ⑦为酯化反应 c.D可以和灼热的CuO发生反应
(7)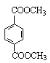 (C10H10O4)的同分异构体中,满足下列条件的有____________种。
(C10H10O4)的同分异构体中,满足下列条件的有____________种。
①能与NaHCO3溶液反应,0.1mol该同分异构体能产生4.48L(标况)CO2气体;
②苯环上的取代基不超过三个;③苯环上的一氯代物只有两种。
 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源:2015-2016学年福建省高一上学期期中测试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.摩尔是国际七个基本物理量之一
B.摩尔质量等于相对分子质量或相对原子质量
C.标准状况下,任何气体的摩尔体积都约为22.4L
D.1mol某种微粒含有的微粒数等于0.012kg12C所具有的碳原子数
查看答案和解析>>
科目:高中化学 来源:2016届辽宁师范大学附属中学高三上学期期中考试化学试卷(解析版) 题型:选择题
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:
CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法不正确的是( )
A.检测时,电解质溶液中的H+向正极移动
B.若溶液中有0.4 mol电子通过,则在标准状况下消耗4.48 L氧气
C.电池反应的化学方程式为:CH3CH2OH+O2==CH3COOH+H2O
D.正极上发生的反应为:O2+4e-+4H+=2H2O
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期期中考试化学试卷(解析版) 题型:选择题
CuO、Fe粉、Fe3O4的混合物中,加一定量稀硫酸,当反应停止后,滤出不溶物,并向滤液中插入一枚铁钉,片刻后.取出铁钉,观察现象。以下结论中正确的是( )
A.若铁钉部分溶解,则滤液中一定含Fe2(SO4)3
B.若铁钉完全溶解,则滤液中一定含CuSO4
C.若铁钉表面有红色物质生成,则不溶物中一定不含Fe
D.若铁钉无变化,则不溶物中一定含Fe
查看答案和解析>>
科目:高中化学 来源:2016届江西上高第二中学高三12月月考理科综合化学试卷(解析版) 题型:选择题
化学与人类生活密切相关,下列与化学有关的说法正确的是( )
A.温室效应是当今世界面临的环境问题,使温室效应增强的气体只有二氧化碳
B.侯氏制碱法的工艺过程中主要应用了物质熔沸点的差异
C.家庭用的“84”消毒液与洁厕灵不能同时混合使用,否则会发生中毒事故
D.实验室里熔化氢氧化钠时,可选用石英坩埚和铁坩埚
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江哈尔滨师大附中高三上学期期中考试化学试卷(解析版) 题型:选择题
将足量CO2通入下列各溶液中,所含离子还能大量共存的是
A.K+、SiO32-、Cl-、NO3- B.H+、NH4+、Al3+、SO42-
C.Na+、S2-、OH-、SO42- D.Na+、C6H5O-、CH3COO-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2016届贵州遵义航天高中高三上学期第三次模拟理综化学试卷(解析版) 题型:简答题
1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才。现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用如下反应模拟哈伯合成氨的工业化生产:N2(g)+3H2(g) 2NH3(g) △H<0
2NH3(g) △H<0
当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如下图所示。

回答下列问题:
(1)已知:①NH3(g)  NH3(g) △H1
NH3(g) △H1
②N2(g)+3H2(g) 2NH3(l) △H2
2NH3(l) △H2
则反应N2(g)+3H2(g) 2NH3(g)的△H= (用含△H1、△H2的代数式表示)。
2NH3(g)的△H= (用含△H1、△H2的代数式表示)。
(2)合成氨的平衡常数表达式为____ ,平衡时,M点NH3的体积分数为10%,则N2的转化率为 (保留两位有效数字)。
(3)X轴上a点的数值比b点 (填“大”或“小”)。上图中, Y轴表示 (填“温度”或“压强”),判断的理由是 。
(4)若将1mol N2和3mol H2分别投入起始容积为1L的密闭容器中,实验条件和平衡时的相关数据如下表所示:

下列判断正确的是____。
A.放出热量:Ql< Q2< △Hl B. N2的转化率:I> III
C.平衡常数:II >I D.达平衡时氨气的体积分数:I>II
(5)常温下,向VmL amoI.L-l的稀硫酸溶液中滴加等体积bmol.L-l 的氨水,恰好使混合溶液呈中性,此时溶液中c(NH4+)__c(SO42-)(填“>”、“<”或“=”)。
(6)利用氨气设计一种环保燃料电池,一极通入氨气,另一极通入空气,电解质是掺杂氧化钇(Y203)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-。写出负极的电极反应式 。
查看答案和解析>>
科目:高中化学 来源:2016届浙江宁波效实中学高三上学期期中考试化学试卷(解析版) 题型:推断题
原子序数依次增大的A、B、C、D、E五种短周期元素,可以两两形成多种原子个数比为1:1的化合物,其中的甲、乙、丙、丁4种化合物有两种属于离子化合物。A、B的原子序数之和是元素D的一半。B既是组成蛋白质的必要元素,也是某些化肥的组成元素。只有C为金属元素,焰色反应呈黄色。请回答下列问题:
(1)元素E 的原子结构示意图为 。
(2)B和D形成的化合物甲,其相对分子质量在170~190之间,且D的质量分数约为70%,则该化合物的化学式为 。
(3)A和B形成的化合物乙为B4A4,在一定条件下可以电离出两种离子,其中一种为10e-的离子,该物质一定条件下的电离方程式为 。
(4)化合物C2D溶液在空气中长期放置会变质生成丙C2D2,用化学方程式表示该过程 。
(5)D和E形成的化合物丁中所有原子均满足8电子稳定结构,该化合物的电子式为 ;该物质遇水剧烈反应,产生有刺激性气味的混合气体X和Y,同时还有固体单质产生,已知X是能使品红褪色的气体,Y在标准状态下的密度为1.63g/L,该混合气体相对于H2的密度为21,上述过程对应的化学方程式为 。
某研究小组同学为确定干燥的X和Y混合气体中Y 的存在,设计方案如下:把干燥的X和Y与干燥的NH3混合,出现白烟,则证明有Y气体,你认为此方案 (填“正确”或“不正确”),理由是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016宁夏回族自治银川一中高一上期中考试化学试卷(解析版) 题型:选择题
科学家刚刚发现了某种元素的原子,其质量是ag,12C的原子质量是bg,NA是阿伏加德罗常数的值,下列说法不正确的是
A.该原子的摩尔质量是aNAg/mol
B.Wg该原子的物质的量一定是 mol
mol
C.Wg该原子中含有 个该原子
个该原子
D.由已知信息可得:NA=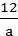
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com