
分析 (1)Cu与氯化铁反应生成氯化铜、氯化亚铁;
(2)铜片在稀硫酸中长时间加热时溶液会呈蓝色,氧气参加反应,生成硫酸铜和水;
(3)Al2O3与焦炭混合后加热并通入氯气,可得到氯化铝,同时生成CO,由反应物、生成物可知反应方程式;
(4)Cu、S元素的化合价升高,N元素的化合价降低,结合电子、原子守恒配平反应;
(5)合金溶于过量盐酸铁和铝反应,剩余固体质量为硅的质量,计算得到n(Si),加入过量氢氧化钠溶液铝离子反应全部变化为偏铝酸钠,铁离子生成氢氧化铁过滤、洗涤得固体.再将所得固体充分加热、灼烧,得红棕色粉末1.60g为Fe2O3,计算得到铁元素物质的量,结合质量守恒计算合金中铝元素物质的量得到化学式.
解答 解:(1)FeCl3蚀刻铜箔反应是三价铁离子具有氧化性和铜反应生成亚铁离子和铜离子,由电子、电荷守恒可知反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+;
(2)因溶液中有氧气,加热能与铜反应生成氧化铜:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO,氧化铜再与硫酸反应:CuO+H2SO4=CuSO4+H2O,两式相加可得2Cu+O2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O,
故答案为:2Cu+O2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O;
(3)根据题意知,反应物是氧化铝、碳和氯气,反应条件是加热,生成物是氯化铝和一氧化碳,所以其反应方程式为:Al2O3+3C+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2AlCl3+3CO,
故答案为:Al2O3+3Cl2+3C$\frac{\underline{\;\;△\;\;}}{\;}$2AlCl3+3CO;
(4)在Cu2S中:
Cu+1→+2↑,失去电子为(2-1)×2
S-2→+6,失去电子为+6-(-2)
化合价共升高10,
而HNO3中N+5→+2化合价降低3,根据化合价的升降守恒:
3Cu2S+□HNO3$\frac{\underline{\;\;△\;\;}}{\;}$□CuSO4+□Cu(NO3)2+10NO↑+( )
再根据原子守恒得:S守恒:3Cu2S+□HNO3$\frac{\underline{\;\;△\;\;}}{\;}$3CuSO4+□Cu(NO3)2+10NO↑+( )
Cu守恒:3Cu2S+□HNO3$\frac{\underline{\;\;△\;\;}}{\;}$3CuSO4+3Cu(NO3)2+10NO↑+( )
N守恒:3Cu2S+16HNO3$\frac{\underline{\;\;△\;\;}}{\;}$3CuSO4+3Cu(NO3)2+10NO↑+( )
质量守恒得:3Cu2S+16HNO3$\frac{\underline{\;\;△\;\;}}{\;}$3CuSO4+3Cu(NO3)2+10NO↑+8 H2O
故答案为:3;16;3;3;10;8;H2O;
(5)准确称取1.46g该合金粉末,加入过量盐酸溶液,充分反应后过滤,铁和铝全部溶解,测定剩余固体质量0.07g为硅.n(Si)=$\frac{0.07g}{28g/mol}$=0.0025mol,向滤液中滴加足量NaOH浓溶液,铝离子反应生成偏铝酸钠,充分搅拌、过滤、洗涤得固体.判断为Fe(OH)3,再将所得固体充分加热、灼烧,得红棕色粉末1.60g为Fe2O3,铁的物质的量n(Fe)=$\frac{1.60g}{160g/mol}$×2=0.02mol,n(Al)=$\frac{1.46g-0.07g-0.02mol×56g/mol}{27g/mol}$=0.01mol;
n(Fe):n(Al):n(Si)=0.02:0.01:0.0025=8:4:1,所以化学式为Fe8Al4Si,
故答案为:Fe8Al4Si.
点评 本题考查常见金属及化合物的性质,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的综合应用,(5)中计算为解答的难点,题目难度中等.


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ②③④⑥ | C. | ①③④⑤ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合物中Fe和Cu的物质的量之比为3:2 | |
| B. | 消耗NaOH溶液体积为260mL | |
| C. | 所得沉淀的质量m=9.83g | |
| D. | 混合物消耗HNO3的物质的量为0.46mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| v正 | v逆 | 平衡常数K | 转化率α |
| [CO2]/mol•L-1 | [H2]/mol•L-1 | [CH4]/mol•L-1 | [H2O]/mol•L-1 | |
| 平衡Ⅰ | a | b | c | d |
| 平衡Ⅱ | m | n | x | y |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
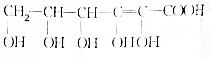 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
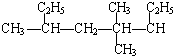 3,5,5-三甲基辛烷
3,5,5-三甲基辛烷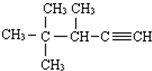 3,4,4-三甲基-1-戊炔
3,4,4-三甲基-1-戊炔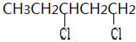 1,3-二氯戊烷
1,3-二氯戊烷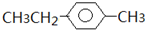 1-甲基-4-乙基苯
1-甲基-4-乙基苯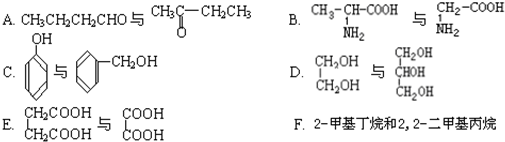
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
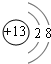 ,非金属性最强的是F.
,非金属性最强的是F.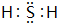 ;含有化合价为+1价的⑦的具有漂白性的一种含氧酸
;含有化合价为+1价的⑦的具有漂白性的一种含氧酸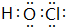 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
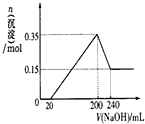 A、B、C、D均为中学化学中常见的物质,它们之间转化关系如图(部分产物已略去):A$→_{一定条件}^{+D}$B$→_{一定条件}^{+D}$C
A、B、C、D均为中学化学中常见的物质,它们之间转化关系如图(部分产物已略去):A$→_{一定条件}^{+D}$B$→_{一定条件}^{+D}$C查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com