
| A. |  表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. |  图中曲线表示反应2SO2 (g)+O2 (g)?2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化 | |
| C. |  表示10 mL 0.01 mol•L-1KMnO4 酸性溶液与过量的0.1 mol•L-1H2 C2 O4溶液混合时,n(Mn2+) 随时间的变化 | |
| D. | 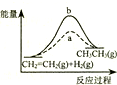 图中a、b曲线分别表示反应CH2=CH2 (g)+H2 (g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化 |
分析 A、盐酸滴定氢氧化钠,PH先下降后突变;
B、因反应为放热反应,则升高温度,平衡逆向移动,平衡后升温K逆减小,而K正增大,且正逆反应的平衡常数互为倒数关系;
C、10 mL 0.01 mol•L-1KMnO4 酸性溶液与过量的0.1 mol•L-1H2 C2 O4溶液混合时发生氧化还原反应生成草酸钾,草酸锰、二氧化碳和水,
D、因该反应是放热反应,应反应物的总能量大于生成物的总能量;
解答 解:A、0.1mol•L-1NaOH溶液的pH为13,用0.1mol•L-1盐酸滴定恰好中和时pH为7,因浓度相同,则体积相同,但酸碱中和在接近终点时,pH会发生突变,曲线的斜率会很大,故A错误;
B、因反应为放热反应,则升高温度,平衡逆向移动,平衡后升温K逆减小,而K正增大,且正逆反应的平衡常数互为倒数关系,故B正确;
C、该反应是放热反应,反应生成的Mn2+对该反应有催化作用,故反应速率越来越快,不是恒定速率,故C错误;
D、图象a活化能减小,a使用了催化剂,因该反应是放热反应,应反应物的总能量大于生成物的总能量,但图象描述是吸热反应,故D错误;
故选B.
点评 本题以图象与中和滴定、化学平衡、氧化还原反应、反应中的能量变化来考查学生,这些知识点是新课程改革考查的重点,明确考点“形变神不变”,做到善于抓规律、编网络来掌握即可,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 试剂a是铁、试剂b是稀硫酸 | |
| B. | 操作I、操作Ⅱ、操作Ⅲ所用仪器相同 | |
| C. | 试剂c是氯气,相应的反应为:2Fe2++Cl2═2Cl-+2Fe3+ | |
| D. | 用酸性KMnO4溶液可检验溶液W中是否还有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+ → → | B. | Na×+ →Na →Na | ||
| C. | Mg${\;}_{×}^{×}$+2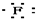 →Mg2+ →Mg2+ | D. |  +${\;}_{×}^{×}$C${\;}_{×}^{×}$ +${\;}_{×}^{×}$C${\;}_{×}^{×}$ → → |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①⑤ | B. | 只有③④⑤ | C. | 只有①②③⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XYZ2 | B. | XYZ3 | C. | X2YZ2 | D. | X2YZ3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24 L Cl2通入足量NaOH溶液中,反应转移电子的数目为0.2NA | |
| B. | 1 mol K与足量O2反应,生成K2O、K2O2和KO2的混合物时转移的电子数为NA | |
| C. | 常温常压下,1.7 g H2O2中含有的电子数为NA | |
| D. | 标准状况下,1 mol CO2所含共用电子对数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com