
【题目】以下是有关SO2、Cl2的性质实验.
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质. 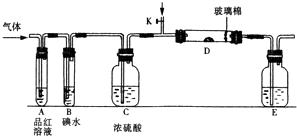
若从左端分别通入SO2和Cl2 , 装置A中观察到的现象是否相同?(填“相同”或“不相同”); 若装置D中装的是五氧化二钒(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为E中盛有溶液.
(2)若装置B中装有5.0mL 1.0×10﹣3mol/L碘水,当通入足量Cl2完全反应后,共转移了5.0×10﹣5mol电子,该反应的化学方程式为 .
(3)某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母) , 则可以看到白色沉淀产生.
A.氨水
B.稀盐酸
C.稀硝酸
D.氯化钙.
【答案】
(1)相同;2SO2+O2  2SO3;NaOH
2SO3;NaOH
(2)5Cl2+I2+6H2O=2HIO3+10HCl
(3)AC
【解析】解:(1)①二氧化硫能和有色物质反应生成无色物质,所以二氧化硫有漂白性;氯气和水反应生成次氯酸,次氯酸具有强氧化性,能使有色物质褪色,所以若从左端分别通入SO2和Cl2 , 装置A中观察到的现象相同,都使品红褪色;二氧化硫和氧气在五氧化二钒作催化剂、加热条件下能发生氧化还原反应生成三氧化硫,反应方程式为 2SO2+O2  2SO3 , E为尾气处理,吸收多余的SO2和Cl2应盛有氢氧化钠溶液,所以答案是:相同;2SO2+O2
2SO3 , E为尾气处理,吸收多余的SO2和Cl2应盛有氢氧化钠溶液,所以答案是:相同;2SO2+O2  2SO3;NaOH;
2SO3;NaOH;
(2.)若装置B中装有5.0mL 1.0×10﹣3mol/L的碘水,当通入足量Cl2完全反应后,转移的电子为5.0×10﹣5mol,令碘元素在氧化产物中的化合价为a,则根据电子转移守恒有5.0×10﹣3L×1.0×10﹣3mol/L×2×a=5.0×10﹣5mol,解得a=+5,所以碘单质被氧化为HIO3 , 则该反应的化学方程式为5Cl2+I2+6H2O=2HIO3+10HCl,所以答案是:5Cl2+I2+6H2O=2HIO3+10HCl;
(3.)将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量试剂仍然无法观察到沉淀产生,说明不发生反应:A、氨水加入后生成亚硫酸铵,亚硫酸根和钡离子生成沉淀,故A正确;B、稀盐酸加入后不反应,故B错误;C、稀硝酸溶液具有强氧化性,将二氧化硫氧化成硫酸根,与钡离子生成硫酸钡沉淀,故C正确;D.氯化钙溶液和二氧化硫不反应,故D错误;所以答案是:AC.
【考点精析】解答此题的关键在于理解氯气的化学性质的相关知识,掌握氯气的化学性质:与金属反应将金属氧化成高价态;非金属反应;与水反应;与碱反应;与还原性物质反应.


 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
【题目】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:
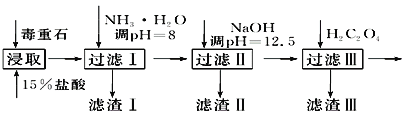
(1)毒重石用盐酸浸取前需充分研磨,目的是_______________________________________;实验室用37%的盐酸配制15%的盐酸,除量筒外还需使用下列仪器中的________。
a.烧杯 b.一定容积的容量瓶 c.玻璃棒 d.滴定管
(2)查阅有关资料获得沉淀各种杂质离子的pH见下表:
沉淀杂质离子 | Ca2+ | Mg2+ | Fe3+ |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
加入NH3·H2O调节pH=8可除去______(填离子符号);滤渣Ⅱ中含__________(填化学式)。加入H2C2O4时应避免过量,原因是_____________________(已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9)。
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。已知:2CrO![]() +2H+===Cr2O
+2H+===Cr2O![]() +H2O Ba2++CrO
+H2O Ba2++CrO![]() ===BaCrO4↓
===BaCrO4↓
步骤Ⅰ.准确移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入几滴酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL。
步骤Ⅱ.准确移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ 相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。
滴加盐酸标准液时应用酸式滴定管,“0”刻度位于滴定管的________(选填“上方”或“下方”)。BaCl2溶液的浓度为________________mol·L-1,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,则所测得Ba2+浓度测量值将________(选填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或操作正确的是( )
A. 用20mL量筒量取15mL酒精,加水5mL,配制质量分数为75%的酒精溶液(P<1)
B. 在200mL某硫酸盐溶液中,含有1.5NA个硫酸根离子,同时含有NA个金属离子,则该硫酸盐的物质的量浓度为2.5mol·L-1
C. 实验中需用2.0mol·L-1的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分数分别为950mL、201.4g
D. 实验室配制500mL 0.2mol·L-1的硫酸亚铁溶液,其操作是:用天平称15.2g绿矾(FeSO47H2O),放入小烧杯中加水溶解,转移到500mL容量瓶、稀释、定量、摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炼金厂的废水中含有CN﹣有剧毒,其性质与卤素离子相似,还原性介于I﹣与Br﹣之间,HCN为弱酸.下列说法不正确的是
A.CN﹣可以和稀硫酸反应生成HCN
B.CN﹣可被Cl2氧化成(CN)2
C.在水溶液中(CN)2可被F﹣还原
D.常温下NaCN溶液显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸工业产生的废气A(主要成分:SO2、O2、N2、CO2等)排放到空气中会污染环境。某化学兴趣小组对废气A的组成进行探究,请回答下列问题。
(1)同学甲设计实验检验废气A中含有CO2,应选择的试剂有_________。
A.NaOH溶液 B.酸性KMnO4溶液 C.澄清石灰水 D.盐酸
(2)同学乙欲测定废气A中SO2的含量,取a L废气A并设计了如下装置进行实验。

①为了保证实验成功,装置A应具有的现象是___________,搅拌的目的是___________。
②同学丙认为A装置前后的质量差就是a L废气中含有的SO2的质量,然后进行含量计算。经小组讨论后,同学丁提出疑问,按照同学丙的实验,若废气中SO2完全被吸收,则最后测定的结果应该偏大,同学丁推断的理由是_______________________________。
(3)兴趣小组的同学查阅资料发现可利用硫酸工业废气A制备皓矾(ZnSO4·7H2O)。实验模拟制备皓矾工业流程如下:

①氧化中加入硫酸铁发生反应的离子方程式是____________________。
②加入Zn粉的目的是_________________________________。
③固体A主要成分是__________________。
④操作b得到纯净皓矾晶体,必要的操作是蒸发浓缩、__________、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关环境保护的说法中错误的是( )
A. 研制开发燃料电池汽车,消除机动车尾气污染
B. 加大石油、煤炭的开采速度,增加化石燃料的供应量
C. 含甲醛、苯及其同系物的装修材料对人体有害
D. 随意丢弃废旧电池会造成重金属盐对土壤和水源的污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】连二亚硫酸钠(Na2S2O4)又称保险粉,是白色砂状或淡黄色粉末固体,己知连二业硫酸钠在碱性条件下较稳定,易被空气氧化,不溶于甲醇,遇水迅速分解,某同学设计利用如下图所示的实验装置制备一定量的连二亚硫酸钠,装置C中的试剂为甲酸钠(HCOONa)、NaOH 的甲醇溶液,回答下列问题:
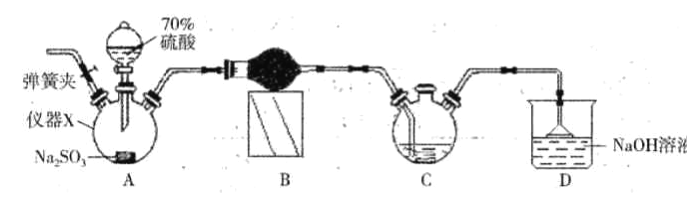
(1)仪器X的名称是_____。装置B中的球形干燥管中盛装的试剂是_______。
(2)装置D的作用是___________。实验时需要将C中温度控制在70-75℃,最好的控制方法是__________。
(3)实验开始时先打开装置A中的弹簧夹通入一段时间N2的目的是______。实验过程中装置C 中除有气体产生外,还能观察到的实验现象为____________。
(4)有同学通过仔细思考后认为,还应在C、D 之间添加一个装置,才能确保C中生成能稳定存在的连二亚硫酸钠,则该装置应具有的功能是______。为得到较纯的连二亚硫酸钠,需要对在过滤时得到的连二亚硫酸钠进行洗涤,洗涤的方法是_________。
(5)若实验中所用Na2SO3的质量为12.6g (硫酸是过量的),最终得到m g干燥的连二亚硫酸钠,则连二亚硫酸钠的产率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香族化合物A是一种基本化工原料,可以从煤和石油中得到。OPA是一种重要的有机化工中间体。A、B、C、D、E、F(聚合物)和OPA的转化关系如下所示: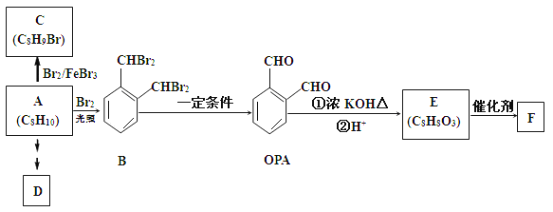
已知:![]()
回答下列问题:
(1)A的化学名称是_________________;
(2)由A生成B的反应类型是______________.在该反应的副产物中,与B互为同分异构体的化合物的结构简式为________________;
(3)写出C所有可能的结构简式_________________________________________________________;
(4)D(邻苯二甲酸二乙酯)是一种增塑剂。请用A和不超过两个碳的有机物及合适的无机试剂为原料,经两步反应合成D。用结构简式表示合成路线:________________________________。
合成路线流程图示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2![]()
![]()
(5)E→F的化学方程式为______________________________________________。
(6)芳香化合物G是E的同分异构体,G分子中含有醛基、酯基和醚基三种含氧官能团,G可能的同分异构体有_______种,写出核磁共振氢谱中峰面积比3∶2∶2∶1的化合物的结构简式___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com