(2011?烟台模拟)某化学小组利用下图装置完成Fe
2O
3 和CO的反应.
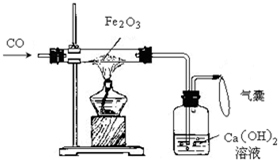
(1)实验开始前,首先必须进行的操作为
检查装置的气密性
检查装置的气密性
.实验开始时,通入CO气体和加热的先后顺序为
先通入CO一段时间,后加热
先通入CO一段时间,后加热
,点燃酒精灯之前,必须检验从装置中排出的CO的纯度.实验过程中,判断反应发生的现象为
红棕色粉末逐渐变黑,澄清石灰水变浑浊
红棕色粉末逐渐变黑,澄清石灰水变浑浊
.
(2)实验时可在酒精灯火焰上罩一个金属网罩,该金属网罩的作用是
提高反应温度
提高反应温度
、
确保受热均匀
确保受热均匀
.若要提高反应温度,还可选用的加热仪器为
酒精喷灯
酒精喷灯
.
(3)查阅资料知,Fe
2O
3和CO进行加热反应,固体质量与反应温度的关系如下图所示.
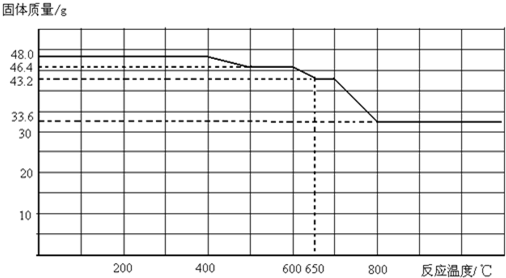
现测得酒精灯对Fe
2O
3加热温度可达到500℃~600℃,则该温度下,Fe
2O
3 的还原产物是
Fe3O4
Fe3O4
.请设计一个简单的实验,证明650℃~700℃时Fe
2O
3的还原产物,简述实验操作和现象
在适量待检物中加入稀H2SO4至完全溶解,再加入少量高锰酸钾溶液,溶液紫色褪去
在适量待检物中加入稀H2SO4至完全溶解,再加入少量高锰酸钾溶液,溶液紫色褪去
.可供选择的试剂:稀H
2SO
4、稀盐酸、KMnO
4溶液、NaOH溶液、KSCN溶液.





 一本好题口算题卡系列答案
一本好题口算题卡系列答案